米国FDA承認済、米国政府も大量調達のihealth抗原検査キットの販売開始について
2月より米国FDA承認済の「ihealth抗原検査キット」の取扱開始が決定致しました。5,000社以上の中国キット生産企業のなか、2社のみ米国FDA承認済で、ihealth社はその1社であります。
この度、株式会社グロックス(本社:東京都中央区 代表取締役:蔡成平、以下「当社」とする)は、中国抗原キット生産の最大手企業である九安医療(Andon Health Co., Ltd.、本社:中国天津、代表取締役:劉毅。及びその子会社であるihealth社。以下「ihealth社」)と提携し、日本販売代理店の権利を取得するようになりました。

抗原検査キット供給不足、または精度低い粗悪品が溢れるなか、当社では2月より米国食品医薬品局(FDA)承認済の抗原検査キット「ihealth」(研究・試験用)の取扱開始を決定致しましたのでご報告致します。
今回、取扱いを開始する「ihealth」(研究・試験用)は、ihealth社により開発製造されており、同社によりおよそ1年間に渡り米国内での臨床試験等を繰り返し実施し、2021年12月22日に米国FDA承認[緊急使用許可(EUA)]を取得し、世界中で承認厳格な米国医薬品規制当局の承認を得た信頼性の高い製品となります。
2022年1月末時点では、数多くある(5,000社以上)抗原検査キットを生産する中国企業の中、2社のみが米国FDA承認(EUA)を取得しており、そのうちの1社がihealth社になります。

【アメリカFDA承認:https://www.fda.gov/media/153925/download】
また、米国連邦政府が全国民へ配布した抗原検査キットは、その大半はihealth社の製品であります。
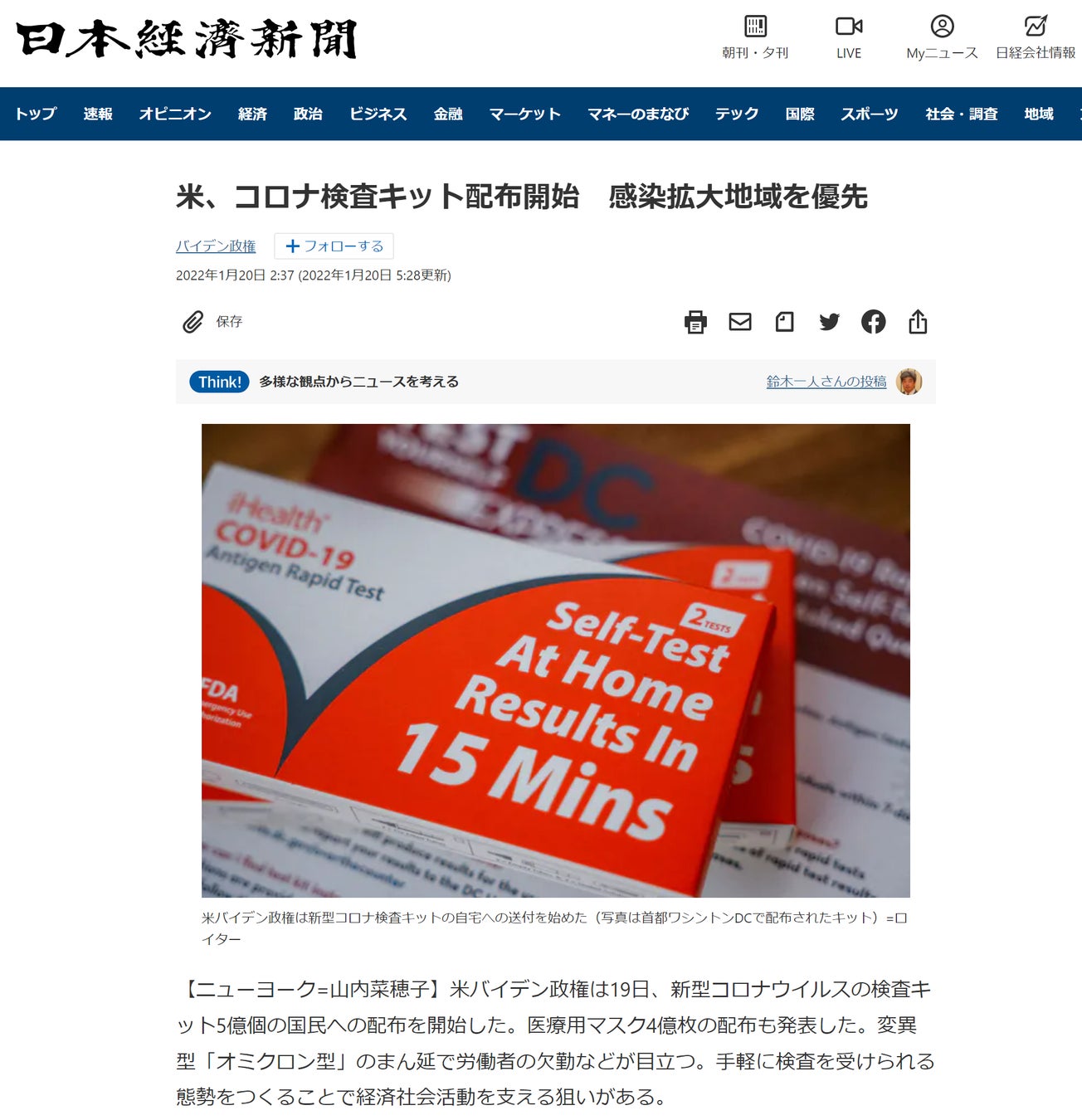
【日本経済新聞 → https://www.nikkei.com/article/DGXZQOGN19E890Z10C22A1000000 】
米国陸軍契約管理本部(U.S.Army Contracting Command)も直近でこのihealth社へ、3.54億回分抗原検査キットの発注を決定しております。
それゆえ、米国連邦政府機関への抗原検査キットの供給について、ihealth社が最大規模の会社となります。


なお、今回取り扱いを開始する「ihealth」(研究・試験用)は、鼻腔ぬぐい液で検査するタイプを予定しており、正式な販売開始日については、決定次第改めてご案内いたします。
ほか、当社は厚生労働省の増産要請を受けて、既に東京都庁や多くの県庁へ納入致しましたパルスオキシメータを2月は可能な限り生産拡大し、2月下旬まで20万台以上の供給できますように目指しています。
抗原検査キットやパルスオキシメータのおまとめ買いをご希望の自治体、企業・団体様及び、本製品のお取り扱いを希望する代理店様や小売店様は是非お問い合わせ下さいませ。
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザーログイン既に登録済みの方はこちら
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
