製薬会社が開発販売する新型コロナウィルスIgM/IgG抗体検査キット販売のご案内【日本バイオテクノファーマ株式会社】
少量の血液で検査可能&5~15分で結果判定。国内外にて2,000例以上の臨床試験データを保有。FDAの使用許可(EUA)を取得済。感染初期及び過去の感染履歴が確認できます。
新型コロナウイルス感染症(COVID-19)「第3波」の到来による感染が急速に拡大する中、本格的な冬の到来により更なる感染拡大が予想されます。医療機関や介護施設における大規模クラスターの発生も目立ち始める中、早期発見・早期対応が重要になります。
PCR検査「陰性」が意味するところは、検査時の前1週間程度は感染していないことであり、2週間前に感染していた可能性や検査直後からの感染可能性は否定することができません。
無症状者の検査を拡大して、陽性者の入院や隔離を行うことは、医療従事者に過大な負担をかけ、活動を制限することは社会全体にとって大きな損失に繋がります。
無症状者の抗体検査を実施することにより、より正確に過去の陽性患者を捉え、偽陰性によるクラスター等の回避にもつながると考えます。


◆◆製品概要◆◆
・原理:金コロイドイムノクロマトグラフィー・検体:血清/血漿/全血/指先血
・判定時間:5~15分
・保管条件:4~30℃
・有効期間:製造後24ヶ月
・登録認証:米国FDA(食品医薬品局)緊急使用許可(EUA)/CEマーク(EU加盟国基準適合)
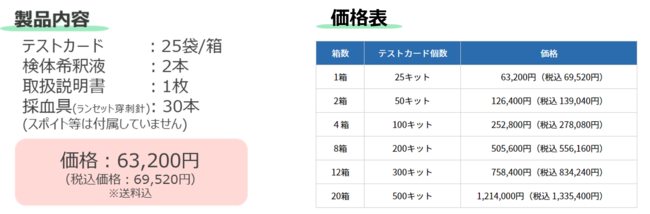
◆◆キット内容◆◆
・テストカード:25キット/箱
・検体希釈液:2本
・取扱説明書:1枚
・採血具(ランセット穿刺針)30本
※スポイト等は付属していません
◆◆使用方法・判定結果◆◆
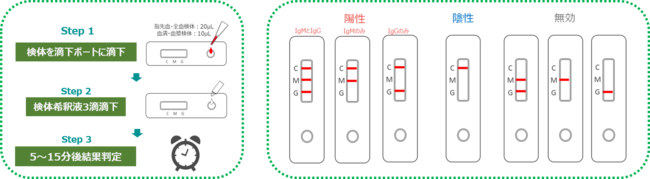
◆◆臨床成績◆◆
核酸検査キットとの評価比較検討
臨床症状発現からの経時的な抗体陽性率の変動成績
新型コロナウイルスの臨床症状の発現から検体採取までの期間において、本検査キットとRT-PCR試薬の分析能を二重盲検臨床試験で比較したもの。そのうちRT-PCRで陽性結果となった128症例における、臨床症状の発現からの経時的な抗体陽性率の変動成績で、本検査キットはRT-PCRとの間に臨床発現からの経時的な強い一貫性・整合性を持つことが示されました。(詳しい内容は弊社HPに掲載しております)
◆◆ご注文について◆◆
本検査キットは、体外診断用医薬品ではありません。
新型コロナウイルスの抗体の有無を見るための研究用試薬としての使用に限定されます。
そのため納品先は医療機関、研究機関、自治体、企業等にご所属されている方に限ります。
本検査キットの購入・使用により発生した損害および損失について、弊社では責任を負いません。
商品購入後の返品・キャンセル等はお受け致しかねます。
ご注文は箱単位(25キット/箱)で承ります。(20箱以上のご注文でお値引き致します)
お支払い方法は、銀行振込となります。(商品発送の際に請求書を同梱いたしますので、到着後10日以内に振込をお願い致します。)
弊社HPからのご注文⇒ https://www.japanbiotechnopharma.com/antibody_test_kit/
FAXでのご注文⇒ 03-6231-0859
◆◆お問い合わせ先◆◆
日本バイオテクノファーマ株式会社
東京都中央区日本橋本町2-6-13
E-mai:info@japanbiotechnopharma.com
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
