国産HAT細胞によるAAV製造プラットフォームの確立
― 遺伝子治療の実用化と普及に向けた新たな一歩 ―
【研究成果のポイント】
-
国産ヒト由来細胞株HAT(Human Amniotic epithelial cell line for gene and cell Therapy)細胞※1を用いることで、高い生産性で空粒子が少ない高品質なアデノ随伴ウイルスベクター(AAV)※2製造プラットフォームを確立。
-
従来の AAV 製造では、生産性と品質の両立が難しく、特に治療効果を持たない空粒子の大量生成とその除去が大きな課題だったが、HAT 細胞の特性と実験計画法(DoE)※3を組み合わせることで、この課題を解決。
-
最先端の分析技術を含む包括的な品質評価により、HAT 細胞で製造した AAV が、従来のAAV と同等の物性・品質を有することを確認。
-
本成果は、遺伝子治療薬の製造コスト低減と安定供給が可能となることで、希少疾患を含む幅広い遺伝子治療薬の臨床開発および実用化への応用が期待。
概要
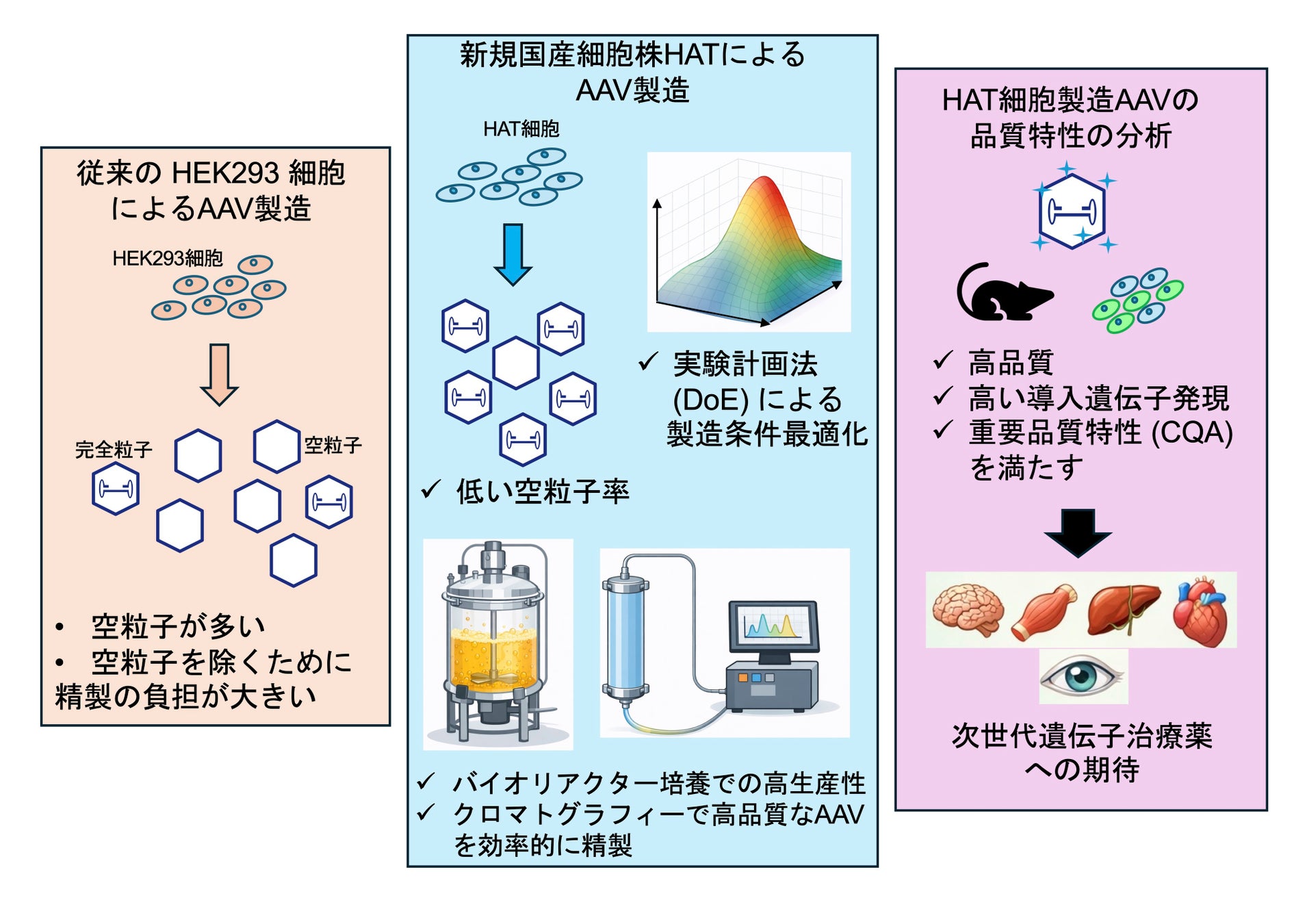
大阪大学大学院工学研究科の津中康央特任准教授(常勤)、内山進教授らの研究グループは、株式会社ちとせ研究所、株式会社ユー・メディコ、自治医科大学、群馬大学、産業技術総合研究所、国立成育医療研究センター、次世代バイオ医薬品製造技術研究組合との共同研究で、新規国産ヒト由来細胞株であるHAT細胞を用いて製造された遺伝子治療用ウイルスベクター(アデノ随伴ウイルスベクター:AAV)が高品質で、かつ高生産性であることを世界で初めて明らかとし、HAT細胞によるAAV製造プラットフォームを確立しました (図1)。
これまで、遺伝子治療用AAVの製造においては、生産性と品質の両立が困難であると考えられており、特に治療効果を持たない空粒子の生成を低減する有効な手法は非常に限られていました。
今回、研究グループは、HAT細胞を用いたAAV製造において、実験計画法(DoE)による製造条件の最適化およびバイオリアクターを用いた培養・製造を行うことで、高い生産性を維持しながら空粒子の生成を大幅に抑制できること、さらに包括的な重要品質特性 (CQA) ※4評価により、得られたAAVが高い品質特性を有することを明らかとし、HAT細胞によるAAV製造プラットフォームを確立しました。
本研究成果により、遺伝子治療薬の製造工程の効率化やコスト低減、さらには高品質な遺伝子治療薬の安定供給が可能となり、臨床開発および実用化の加速が期待されます。
本研究成果は、米国科学誌「Molecular Therapy Advances」に、2026年2月15日(日)に公開されました。
【内山教授のコメント】
遺伝子治療に用いられるウイルスベクターには極めて高い品質が求められる一方で、その製造には高いコストと専門的な製造基盤が必要であるという課題がありました。
今回、国産の細胞株である HAT細胞 を用いたAAV製造プラットフォームの構築に成功したことで、日本国内において高品質な遺伝子治療用ベクターを、コストを抑えながら安定的に製造・供給する体制の実現に向けた大きな一歩を踏み出しました。臨床応用や実用化に向け、より多くの患者さんへ遺伝子治療を届けるための基盤となることが期待されます。
研究の背景
AAVは、現在、世界で8つの遺伝子治療薬が承認されており、次世代医療を支える基盤技術として大きな注目を集めています。しかし、遺伝子治療薬の臨床応用を成功させるためには、安全性と品質を両立したAAVを、効率的かつ低コストで製造する技術の確立が不可欠です。これまで、遺伝子治療用AAVの製造には、主に昆虫細胞またはヒト由来のHEK293細胞が用いられてきました。昆虫細胞による製造は高い生産性を有する一方で、翻訳後修飾の違いなどに起因する品質や安全性の観点で課題が指摘されています。一方、ヒトHEK293細胞で製造されたAAVは、昆虫細胞由来のものと比べて高品質であるとされていますが、生産性が低いという課題があります。さらに、昆虫細胞でもHEK293細胞でも、治療に必要な目的導入遺伝子を含まず、治療効果を持たない空粒子AAVが多く生成されることが知られており、これらの空粒子の混入は治療効果を低減し、予想外の免疫反応を誘導する可能性があるため、その除去が製造における大きな課題となっています。
研究の内容
研究グループでは、最近開発された国産の新規ヒト由来細胞株であるHATを用いて、AAVの製造を行いました。AAVの製造条件の最適化には実験計画法(Design of Experiments:DoE)を用い、高生産性を維持しつつ、治療効果を持たない空粒子の生成を抑制できる製造条件を探索しました。その結果、HAT細胞を用いたAAV製造において、空粒子の生成を低減しながら高い生産性を実現する最適条件を見出しました。この最適条件下で製造されたHAT細胞由来AAVは、同様にDoEを用いて最適化した条件で製造された従来のヒトHEK293細胞由来AAVと比較して、高い生産性を示すことが明らかになりました。さらに、バイオリアクターを用いた大規模培養においても、HAT細胞は高い生産性を示し、スケールアップ製造への高い適用性が確認されました。また、HAT細胞で製造されたAAVは、もともと空粒子の生成が少ないことから、臨床製造で一般的に用いられるアフィニティークロマトグラフィーおよび陰イオン交換クロマトグラフィーによる精製工程において、空粒子がほぼ除去され、高品質なAAVを効率的に精製できることが確認されました。加えて、精製後のAAVについて、空粒子率、翻訳後修飾、導入遺伝子の発現能など、遺伝子治療薬として重要品質特性 (CQA)を包括的に評価した結果、HAT細胞由来AAVが既存のHEK293細胞由来製品と同等、あるいは一部ではそれを上回る品質特性を示すことを確認しました。
以上の結果から、本研究によって、HAT細胞が臨床試験用の高品質AAVを高生産性で製造可能な有望な細胞株であることを示すとともに、HAT細胞由来高品質AAVの最適な製造条件およびCQAを明確とし、製造プラットフォームを確立しました。
本研究成果が社会に与える影響(本研究成果の意義)
本研究成果は、遺伝子治療薬の実用化における最大の課題の一つである「高品質AAVの安定かつ効率的な供給」に対し、新たな解決策を提示するものです。HAT細胞を用いたAAV製造プラットフォームは、高い生産性と低い空粒子生成という特長を併せ持つことから、製造工程の簡素化や精製負担の軽減につながり、遺伝子治療薬の製造コスト低減および安定供給に大きく貢献すると期待されます。これにより、これまで製造面の制約から十分な供給が難しかった希少疾患をはじめとする遺伝子治療薬の臨床開発および実用化の加速が見込まれます。さらに、本研究で明確化した最適な製造条件およびCQAは、研究段階から臨床試験、さらには商用製造への円滑な移行を可能にし、遺伝子治療薬の品質および安全性の向上にも寄与します。
今後は、本研究成果を基盤として、産学官連携による実用化研究を推進し、国内における遺伝子治療薬製造エコシステムの確立を目指します。これにより、国産技術による安定供給体制の構築と、遺伝子治療分野における我が国の国際競争力の強化に貢献していきます。
特記事項
本研究成果は、2026年2月15日(日)に米国科学誌「Molecular Therapy Advances」(オンライン)に掲載されました。
タイトル:“Manufacture of adeno-associated virus vectors by a novel human-derived cell line HAT and comprehensive characterization of the vectors”
著者名:Yasuo Tsunaka, Mitsuko Fukuhara, Saki Shimojo, Aoba Matsushita, Takahiro Maruno, Sereirath Soth, Haruka Nishiumi, Mark Allen Vergara Rocafort, Toshie Kuwahara, Kenjiroo Matsumoto, Kosei Shibata, Ryoji Nakatsuka, Ryo Asahina, Saho Mizukado, Yuuki Fukai, Tomoki Togashi, Nemekhbayar Baatartsogt, Kimitoshi Takeda, Atsushi Kuno, Yuji Kashiwakura, Yuki Yamaguchi, Kazuaki Nakamura, Yugo Hirai, Hirokazu Hirai, Tsukasa Ohmori, Takeshi Omasa, and Susumu Uchiyama
DOI: https://doi.org/10.1016/j.omta.2026.201700
なお、本研究は、日本医療研究開発機構(AMED)の「遺伝子・細胞治療用ベクター新規大量製造技術開発・再生医療・遺伝子治療の産業化に向けた基盤技術開発事業」(助成金JP18ae0201001, JP18ae0201002, JP24se0123004)の助成を受け実施されました。
用語説明
※1 HAT(Human Amniotic epithelial cell line for gene and cell Therapy)細胞
HAT細胞は、ヒトの胎盤に由来する羊膜上皮細胞をもとに開発された、遺伝子・細胞治療用の新規国産ヒト由来細胞株です。高い増殖性能性を示し、遺伝子治療薬の材料となるウイルスベクターを効率よく、かつ安定して作ることができる特徴があります。HAT細胞の樹立に関する報告は、共同研究者である株式会社ちとせ研究所の平井悠吾らによって、Molecular Therapy: Methods & Clinical Development 誌(https://doi.org/10.1016/j.omtm.2025.101594)に掲載されています。
※2 アデノ随伴ウイルスベクター(AAV)
Adeno-associated virus vector。アデノ随伴ウイルスベクターは、病気の治療に必要な遺伝子を体内の細胞へ運ぶために使われる、とても小さなウイルスベクターです。人に対する病原性が低く、安全性が高いことから、遺伝子治療薬の「運び屋 (ベクター) 」として広く利用されています。特に、血友病のように生まれつき遺伝子に異常がある病気の治療や、脳や筋肉、肝臓、目、心臓など、狙った体の部位に遺伝子を届ける体内での遺伝子治療に多く用いられています。また、一度導入した遺伝子が長期間にわたって働き続けるという特長があり、治療効果が長く持続する点も大きな利点です。
※3 実験計画法(DoE)
実験計画法(Design of Experiments:DoE)は、さまざまな条件を効率よく組み合わせて実験を行い、最も良い結果が得られる条件を科学的に見つけ出す方法です。少ない実験回数で、生産量や品質が高くなる条件を明らかにできるため、医薬品の開発や製造に広く用いられています。
※4 重要品質特性(CQA)
Critical Quality Attributes。重要品質特性とは、医薬品が安全で、しっかり効果を発揮するために特に重要とされる品質のポイントのことです。遺伝子治療薬の場合、「目的遺伝子が正しく体内の特定の組織や細胞に届くか」、「治療に不要な成分が少ないか」、「毎回同じ品質で作られているか」などが、重要品質特性として評価されます。
SDGs目標



参考URL
内山進 教授 研究者総覧URL
https://rd.iai.osaka-u.ac.jp/ja/0abc739b66a8f19e.html
津中康央 特任准教授(常勤) 研究者総覧URL
https://rd.iai.osaka-u.ac.jp/ja/ead815e728fd9a41.html

このプレスリリースには、メディア関係者向けの情報があります
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
