【摂南大学】ALSの原因タンパク質TDP-43の新たな機能を発見
【本研究のポイント】
・神経細胞(ニューロン)特異的にTDP-43*1をノックアウト*2したマウスの脳において軸索*3の髄鞘化*4が抑制されていることを発見
・ニューロンのTDP-43がニューレキシン1*5発現の制御を介して軸索の髄鞘化を促進していることを解明

ニューロンのTDP-43はニューレキシン1のメッセンジャーRNA(mRNA) *6の安定化を介して軸索の髄鞘化を誘導する。
【研究概要】
名古屋大学大学院医学系研究科神経内科学の李佳益 研究員(筆頭著者)、井口洋平 講師、勝野雅央 教授、同分子細胞学の和氣弘明 教授(生理学研究所 教授/クロスアポイントメント)と摂南大学農学部応用生物科学科の芳本玲 准教授らの研究グループは神経細胞(ニューロン)のTDP-43がニューレキシン1発現の調節を介して軸索の髄鞘(ずいしょう)化を制御していることを解明しました。
筋萎縮性側索硬化症(ALS)と前頭側頭葉変性症(FTLD)はニューロンが細胞死を来すことで筋肉が萎縮し、認知機能が低下する進行性の神経変性疾患です。ALSでは最終的には呼吸や嚥下をつかさどる筋肉を含む全身の筋肉が動かせなくなります。ALSの9割以上を占める孤発性ALSの発症原因は未だ不明で、進行を十分に抑制できる治療法は存在しません。ALS/FTLD病態では、TDP-43が変性ニューロンの核から脱出して細胞質に凝集体として過剰に蓄積することがわかっていて、「TDP-43の機能喪失」がニューロン死の主要因の一つと考えられています。また、ALS/FTLDではニューロンの軸索を取り囲む髄鞘が減少していることも知られていましたが、その病態については十分に解明されていませんでした。本研究グループは、ニューロンのTDP-43がニューレキシン1の発現調節を介して軸索の髄鞘化を制御していることを解明しました。
本研究ではニューロン特異的にTDP-43の発現を消失(ノックアウト)させたマウス(TDP-43cKOマウス)の脳を詳細に観察したところ、軸索の髄鞘化が著しく低下していることを発見しました。低髄鞘化の原因を探索したところニューロンのTDP-43がニューレキシン1の発現を調節していること、またそのニューレキシン1が軸索の髄鞘化を制御していることを解明しました。さらに、TDP-43cKOマウスでは短期記憶障害を認めましたが両側の海馬*7のニューロンにニューレキシン1を補充したマウスでは記憶障害の改善がみられました。また、ALS患者剖検脳や脊髄を観察したところ、変性ニューロン内ではニューレキシン1の発現が低下していることも確認しました。本研究で見出された「TDP-43機能喪失状態におけるニューレキシン1発現低下と低髄鞘化」は、ALS/FTLDの病態解明と病態抑止療法へ応用が期待されます。
なお、本研究は名古屋大学、生理学研究所、摂南大学、愛知医科大学、自治医科大学との共同研究により行われました。本研究成果は、2026年2月23日(米国東部時間)の週に、米国科学誌『Proceedings of the National Academy of Sciences』にオンライン掲載予定です。
1. 背景
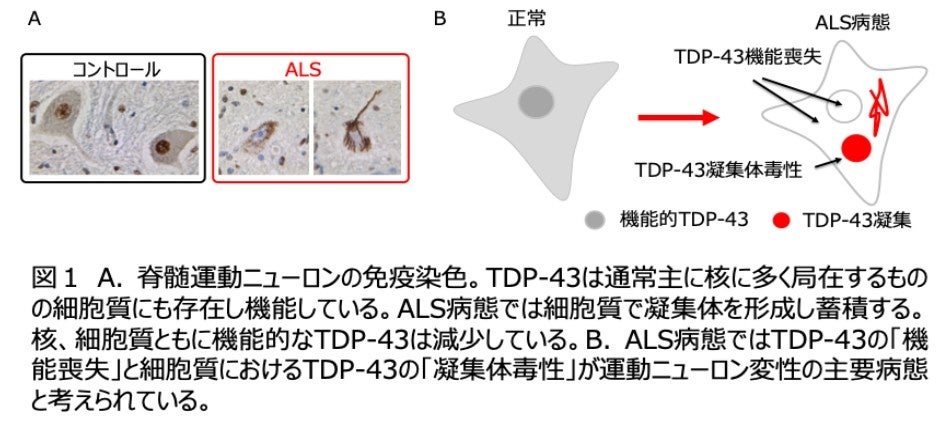
ALS患者の多くは中高年以降に特別な誘因や前兆もなく発症します。病初期は限られた領域の筋力低下に留まりますが、徐々に全身の筋力が低下し、平均3〜5年で呼吸筋麻痺のために自力での呼吸ができなくなります。現在使用可能なALS治療薬は進行を遅らせる効果はありますが病態抑止効果は十分とは言えません。ALS患者の9割以上は血縁者に同様の患者がいない孤発性であり、発症原因が特定されていません。しかし亡くなったALS患者さんの脳や脊髄の病理学的・生化学的解析から、ALSの運動ニューロンでは本来核に存在するTDP-43というタンパク質が核から脱出し細胞質に凝集体を形成することがわかってきました(図1)。また、認知症の一つである前頭側頭葉変性症(FTLD)の約半数では、ALS同様のTDP-43病理を変性ニューロンに認め、ALSとFTLDが合併する症例も一定程度みられます。ALS病態では、TDP-43の「機能喪失」と「凝集体毒性」がニューロン死の主要因と考えられています。ALSにおけるTDP-43異常を正常化できれば良いわけですがTDP-43がこのような異常を来す原因が特定できていないため、現状では「TDP-43の機能を補う」ことと、「凝集体を減らす」ことが現実的な治療戦略となります。
本研究は「TDP-43の機能を補う」ことを目的とする新たな治療戦略を提唱するものです。
2. 研究成果
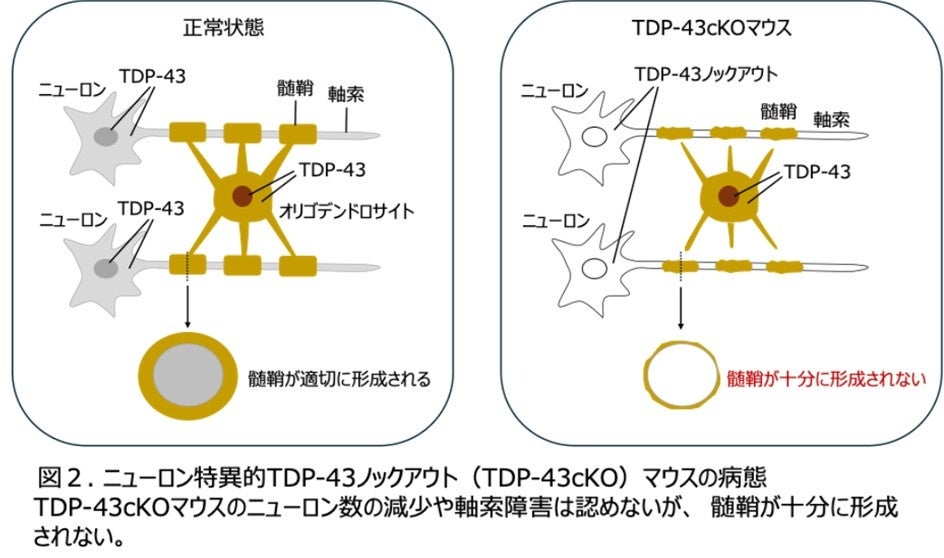
本研究ではニューロンでのみTDP-43を欠失させたマウス(TDP-43cKOマウス)の脳を詳しく調べました。その結果、ニューロンの軸索を取り囲む「髄鞘(ずいしょう)」と呼ばれる構造が減少していることを発見しました(図2)。髄鞘は軸索を包み込み、神経の電気信号を速く正確に伝えるために重要な構造です。このマウスでは、ニューロンそのものや軸索に目立った異常は見られませんでした。このことから、髄鞘の減少は、ニューロンの障害による二次的な変化ではないと考えられました。髄鞘は、ニューロンとは別の細胞であるオリゴデンドロサイト*8という細胞によって作られますが、今回のマウスではオリゴデンドロサイトの数自体は減っていませんでした。
さらに、脳の左右の運動皮質間で神経信号がどのように伝わるかを調べたところ、TDP-43cKOマウスでは信号の伝わりが悪くなっていることが分かりました。また、電子顕微鏡*9で詳しく観察すると、髄鞘が通常より薄くなっていることも確認されました(図3)。今回の研究結果から、ニューロンのTDP-43 が、オリゴデンドロサイト由来の髄鞘形成を制御している可能性が示されました。

ニューロンにおいて、TDP-43がノックアウトされた状態で発現量が変化する分子を探索すると、ニューレキシン1が減少していることがわかりました。また、TDP-43はニューレキシン1のメッセンジャーRNAを安定化することでニューレキシン1の発現量を調節していました(図4)。

そして、ニューレキシン1をTDP-43cKOマウスのニューロンに補充すると髄鞘が有意に回復することもわかりました(図5)。 さらに、TDP-43cKOマウスでは短期記憶障害を認めましたが、両側の海馬のニューロンにニューレキシン1を補充したマウスでは記憶障害の改善がみられました(図6)。
また、ALS患者剖検脳や脊髄を観察したところ、変性ニューロン内ではニューレキシン1の発現が低下していることも確認しました。


3. 今後の展開
本研究ではTDP-43が機能喪失をきたしたニューロンにおいて、ニューレキシン1の発現低下による低髄鞘化や機能障害が生じることが示されました。ニューレキシン1の機能を回復させる治療によってALSやFTLDの病態を改善させることができるかもしれません。今後はTDP-43ノックアウトモデルだけでなくTDP-43凝集体形成を伴うALS/FTLD病態モデルの変性ニューロンにおいてもニューレキシン1関連病態を解析して病態解明、治療薬開発に繋げて行きたいと考えています。
4. 支援・謝辞
本研究は、日本医療研究開発機構(AMED)、科学研究費補助金(日本学術振興会(JSPS))、武田財団、ヒロセ財団の助成を受けて実施されました。
【用語説明】
*1)TDP-43:RNA結合タンパク質。通常は核に多く存在しRNA代謝に関わっている。
*2)ノックアウト:特定の遺伝子の働きを意図的に止めた状態。
*3)軸索:ニューロンの電気信号を遠隔部へ伝える伝導構造。
*4)髄鞘化:軸索を包む膜が作られ、情報が速く伝わるようになる仕組み。
*5)ニューレキシン1: 主に神経細胞の軸索側に存在する細胞接着分子です。シナプス形成・成熟・機能維持や軸索の髄鞘化を制御する。
*6)メッセンジャーRNA(mRNA):遺伝子の情報をタンパク質に作り替えるための情報を翻訳装置へ伝達するRNA。
*7)海馬:脳の側頭葉内側に存在し短期的な記憶を長期的な記憶に変える役割を担っている。
*8)オリゴデンドロサイト:中枢神経内で髄鞘を形成する細胞。
*9)電子顕微鏡:超微細構造を可視化するための解析手法。
*10)電気生理学的検査:神経活動を電気信号として記録し、機能を評価する検査。
【論文情報】
雑誌名:Proceedings of the National Academy of Sciences
論文タイトル:Neuronal TDP-43 regulates myelin formation via Neurexin1 mRNA stabilization
著者:Jiayi Li1, Yohei Iguchi1*, Kenji Yoshida2, Daisuke Kato2, 3, Kunihiko Araki1, 4, Kenta Kobayashi5, Satoshi Yokoi6, Rei Yoshimoto7, Madoka Iida1, Yoshinobu Amakusa1, Yu Kawakami1, Takashi Yoshimura1, Ryo Chikuchi1, Koyo Tsujikawa1, 8, Yuichi Riku1, 9, Yasushi Iwasaki9, Yohei Okada10, Nobuhiko Ohno11, 12, Hiroaki Wake2, 3, Masahisa Katsuno1, 13*
1: Department of Neurology, Nagoya University Graduate School of Medicine
2: Department of Anatomy and Molecular Cell Biology, Nagoya University Graduate School of Medicine
3: Division of Multicellular Circuit Dynamics, National Institute for Physiological Sciences, National Institute of Natural Sciences
4: Institute of Experimental Epileptology and Cognition Research, Medical Faculty, University of Bonn
5: Section of Viral Vector Development, National Institute for Physiological Sciences
6: Department of Pathophysiological Laboratory Sciences, Nagoya University Graduate School of Medicine
7: Department of Applied Biological Sciences, Faculty of Agriculture, Setsunan University
8: Department of Genetics, Research Institute of Environment Medicine (RIeM), Nagoya University
9: Department of Neuropathology, Institute for Medical Science of Aging, Aichi Medical University
10: Department of Neural iPSC Research, Institute for Medical Science of Aging, Aichi Medical University
11: Division of Histology and Cell Biology, Department of Anatomy, Jichi Medical University
12: Division of Ultrastructural Research, National Institute for Physiological Sciences
13: Department of Clinical Research Education, Nagoya University Graduate School of Medicine
*Corresponding authors
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
