セラミドやスフィンゴミエリンを識別する受容体がアナフィラキシーを制御
― 高親和性IgE受容体シグナルの制御メカニズムの解明から治療法開発へ ―
順天堂大学 大学院医学研究科アトピー疾患研究センターの伊沢久未 特任准教授、北浦次郎 教授、奥村康 センター長ら、および浜松医科大学の瀬藤光利 教授、東京大学、理化学研究所、花王株式会社らの共同研究グループは、免疫受容体CD300*¹が生体内脂質のスフィンゴミエリン(SM)やセラミド*²を識別してマスト細胞の高親和性IgE受容体(FcεRI)*³シグナルを制御することによって、アナフィラキシー*⁴の重症度が決まることを明らかにしました。マスト細胞のFcεRIシグナルは、ある種類(I型)のSMを認識する受容体CD300d3*⁵により促進される一方、セラミドや他の種類(Ⅱ型)のSMを認識する受容体CD300f*⁶により抑制されることをマウスモデルで証明しました。本成果は、FcεRIシグナルの制御メカニズムの解明からアナフィラキシーの治療法開発への道を開くものです。
本論文は国際学術誌Cell Reportsのオンライン版に2026年3月4日付で公開されました。
本研究成果のポイント
● 生体内脂質を識別する免疫受容体がアナフィラキシーを制御することをマウスモデルで証明。
● I型スフィンゴミエリンが結合するCD300d3はアナフィラキシーを促進し、セラミドやⅡ型スフィンゴミエリンが結合するCD300fはアナフィラキシーを抑制する。
● 生体内脂質が高親和性IgE受容体シグナルを制御するメカニズムの解明から治療法開発へ。
背景
近年増加している即時型アレルギー(食物アレルギーや花粉症など)の中で最も重篤な病態がアナフィラキシーです。抗原と特異的IgEによりマスト細胞のFcεRIが架橋刺激されると、マスト細胞は活性化してヒスタミンなどを含む顆粒を放出(脱顆粒)し、即時型アレルギーを誘導しますが、全身に及び重篤化するとアナフィラキシーとなります。細胞外領域の相同性が高いCD300fとCD300d3はマスト細胞に発現する免疫受容体です。研究グループはこれまでに、脂質のセラミドを認識するCD300fがFcεRIシグナルを抑制してアナフィラキシーを抑えることを明らかにしましたが、CD300d3の生理的な役割は不明でした。本研究では、CD300d3の機能を明確にするため、CD300d3欠損マウスを作出し、アナフィラキシーモデルを解析しました。さらに、CD300d3やCD300fが識別する脂質の種類を詳しく調べました。
内容
CD300d3の機能を解明するため、CD300d3欠損マウスを作出しました。最初に、CD300d3欠損はマウスの免疫細胞(マスト細胞を含む)の分化や数に影響しないことを確認しました。次に、野生型およびCD300d3欠損マウスの骨髄から誘導したマスト細胞(BMMC)をIgEと抗原で刺激して脱顆粒率を測定しましたが、両者に差はありませんでした。しかし、IgEと抗原による皮膚マスト細胞の脱顆粒に依存する受動的皮膚アナフィラキシー(PCA)*⁷反応を解析したところ、野生型マウスと比較してCD300d3欠損マウスのPCA反応は減弱しました。これらの結果から、CD300d3は生体内でマスト細胞の周囲に存在する何らかの分子を認識してFcεRIシグナルを増強することが示唆されました。
マウスのCD300fとCD300d3の細胞外領域構造が類似すること、CD300fが脂質のセラミドを認識することに着目し、CD300d3が認識する分子の同定を試みました。CD300d3の細胞外領域を利用するアッセイ系を構築し、さまざまな脂質をスクリーニングしたところ、CD300d3はセラミドに結合しないがSMに結合することを見出しました。さらに、炭素や二重結合の数が異なるさまざまなセラミドやSMを調べたところ、CD300d3はSM全般に結合し、CD300fはセラミドとある種類のSMに結合することがわかりました。つまり、SMは機能的に2種類、(CD300d3に結合するがCD300fに結合しない)I型SMと(CD300d3およびCD300fに結合する)Ⅱ型SMに分けられました。実際、質量分析装置で解析し、血清や(マスト細胞が局在する)皮膚の真皮にⅠ型SMとⅡ型SMがともに存在することを確認しました。
セラミドはCD300fに結合しても、それだけでCD300fの抑制シグナル伝達モチーフ(ITIMやITSM)はリン酸化されません。しかし、セラミドとCD300fの結合はIgEと抗原によるBMMCの脱顆粒を抑制します。このとき、セラミドが結合するCD300fは架橋されたFcεRIに近づくため、その下流で活性化したチロシンキナーゼ(LynやSyk)がCD300fのITIMやITSMを効率よくリン酸化し、そこに動員されるチロシンフォスファターゼ(SHP-1やSHP-2)がFcεRIシグナルを抑制します。他方、I型SMだけで刺激してもBMMCは脱顆粒しませんが、I型SM とCD300d3の結合はIgEと抗原によるマスト細胞の脱顆粒を増強することがわかりました。このとき、I型SMが結合するCD300d3は架橋されたFcεRIに近づくため、その下流で活性化したチロシンキナーゼがCD300d3と会合するγ鎖のITAMもリン酸化し、FcεRIシグナルを増強すると考えられました。これらの結果と一致して、セラミドリポソームの投与は野生型とCD300d3欠損マウスのPCA反応を減弱させました(CD300f欠損マウスのPCA反応に影響しませんでした)。また、I型SMリポソームの投与は、野生型とCD300f欠損マウスのPCA反応を増強させました(CD300d3欠損マウスに影響しませんでした)。他方、Ⅱ型SMリポソームの投与は、CD300f欠損マウスのPCA反応を増強する一方、CD300d3欠損マウスのPCA反応を減弱させました。しかし、野生型マウスのPCA反応を減弱させることがわかりました。つまり、Ⅱ型SMが結合するCD300fの抑制シグナルはⅡ型SMが結合するCD300d3の活性化シグナルを凌駕すると考えられました。
これらを総合すると、野生型マウスの定常状態では、セラミドとⅡ型SMが結合するCD300f、I型SMとⅡ型SMが結合するCD300d3、細胞外脂質が結合していないCD300fやCD300d3がマスト細胞上に存在すると考えられます。マスト細胞のFcεRIがIgEと抗原により架橋刺激されると、細胞外脂質の結合したCD300d3やCD300fは架橋されたFcεRIに近づきます。その結果、活性化したLynやSykがCD300d3と会合するγ鎖のITAMをリン酸化するとともに、CD300fのITIMやITSMをリン酸化します。ITAMのリン酸化はFcεRIシグナルを促進し、ITIMやITSMのリン酸化はFcεRIシグナルを抑制するため、このバランスがFcεRIシグナルの強さ、したがって、マスト細胞の活性化(脱顆粒)レベルを決め、最終的なアナフィラキシーの重症度を規定します。したがって、セラミドリポソームの投与はセラミドが結合するCD300fを増加させるため、CD300fの抑制シグナルが増強してアナフィラキシーを抑えると考えられます。また、SMとCD300d3の結合を阻害する薬剤はCD300d3による活性化シグナルを抑制してアナフィラキシーを抑えると考えられます。
今後の展開
アナフィラキシーを含む即時型アレルギーの病態解明には、マスト細胞のFcεRIシグナルを制御する仕組みを理解することが不可欠です。研究グループは、生体内の細胞外脂質であるセラミドやSMを識別する免疫受容体CD300がアナフィラキシーを制御することを明らかにしました。今後、CD300が二重結合や炭素数のわずかに異なる脂質を識別する分子メカニズムの解明を進めながら、マウスとヒトのCD300による脂質認識機構の全貌解明を目指します。同時に、CD300を標的とするアレルギー・炎症性疾患の予防・治療薬の開発を進めます。さらに、本研究にとどまらず、生体内の細胞外脂質による免疫制御機構の解明が進み、免疫疾患に対する創薬につながることが期待されます。
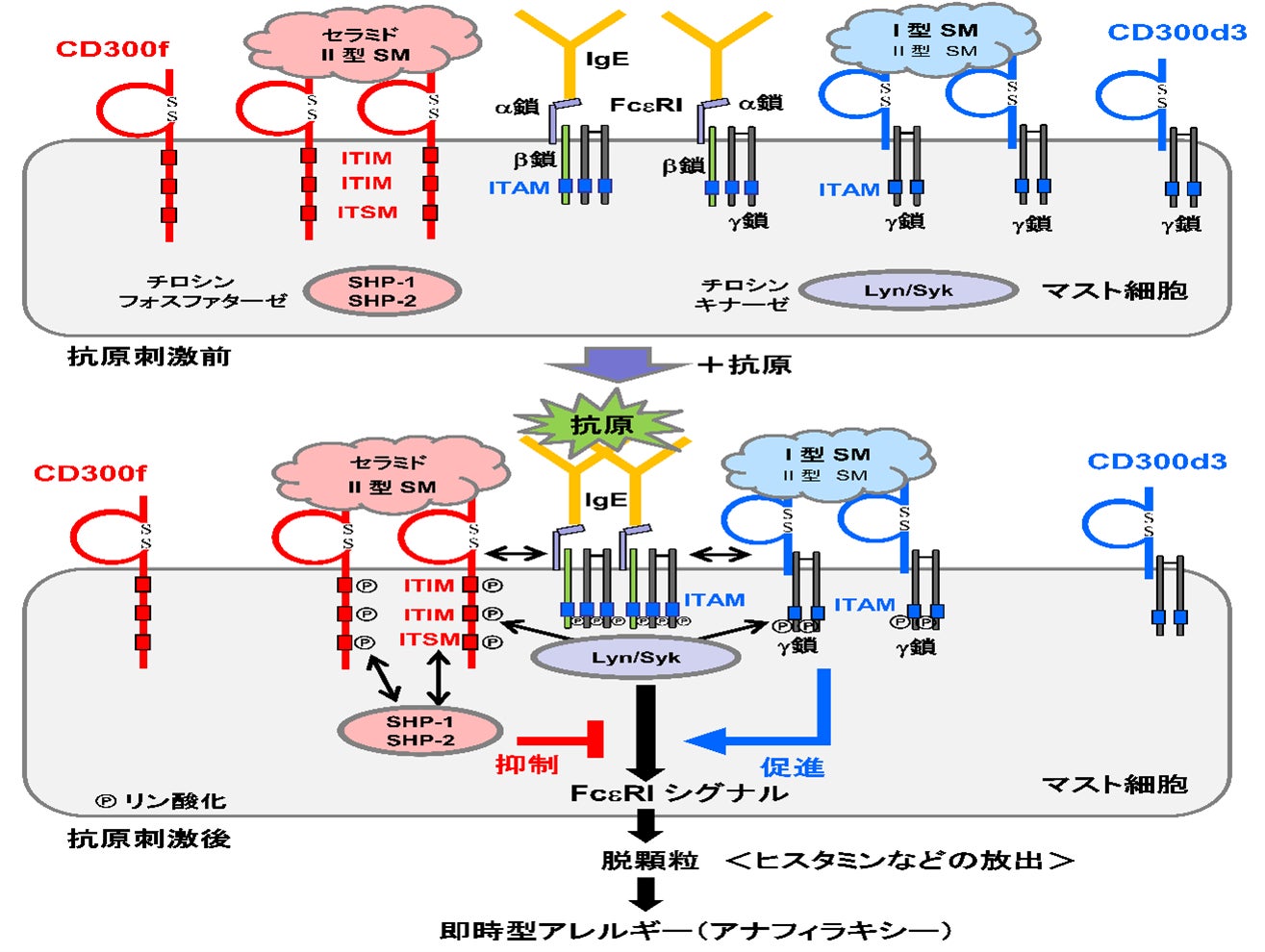
図1:本研究で明らかになったマウスの皮膚アナフィラキシーの制御メカニズム
SMは機能的に、I型<CD300d3に結合するがCD300fに結合しない>とⅡ型<CD300d3とCD300fに結合する>に分けられ、I型SMとⅡ型SMはともにマウスの皮膚真皮に存在します。マスト細胞表面にはFcεRIとともにCD300fとCD300d3が発現しています。定常状態では、セラミドとⅡ型SMが結合するCD300fとI型SMとⅡ型SMが結合するCD300d3が存在します。このとき、CD300d3と会合するγ鎖(FcεRIのγ鎖と同じ分子)のITAMやCD300fのITIMやITSMはリン酸化されていません。抗原特異的IgEはFcεRIのα鎖に結合しますが、それだけでFcεRIシグナルは起動しません。抗原が加わり、IgEを介してFcεRIを架橋すると、FcεRI直下のチロシンキナーゼ(LynやSyk)が活性化し、FcεRIのβ鎖やγ鎖のITAMをリン酸化します。これが引き金となり、FcεRIシグナルは下流に伝わり、マスト細胞は活性化します。放出される顆粒はヒスタミンを含み、マウスの皮膚の血管透過性を亢進させて皮膚アナフィラキシーを誘導します。このとき、セラミドやⅡ型SMが結合しているCD300fは架橋されたFcεRIに近づくため、直下で活性化したLynやSykがCD300fのITIMやITSMをリン酸化します。そこに動員されるチロシンフォスファターゼ(SHP-1やSHP-2)がFcεRIシグナルを抑制します。他方、I型SMやⅡ型SMが結合しているCD300d3も架橋されたFcεRIに近づくため、活性化したLynやSykはCD300d3の会合するγ鎖のITAMもリン酸化してFcεRIシグナルを促進します。つまり、CD300d3とCD300f はFcεRIの活性化シグナルを正負に制御し、それぞれアクセルとブレーキの役割を果たします。また、I型SMリポソームを投与するとCD300d3シグナルを介してアナフィラキシーは増強し、セラミドリポソームを投与するとCD300fシグナルを介してアナフィラキシーは抑制されます。興味深いことに、CD300d3とCD300fの両方に結合するⅡ型SMリポソームを投与するとアナフィラキシーは抑制されます。つまり、Ⅱ型SMの存在下では、CD300fの抑制シグナルはCD300d3の活性化シグナルを凌駕します。したがって、I型SMはCD300d3を介してアナフィラキシーを促進し、セラミドとⅡ型SM はCD300fを介してアナフィラキシーを抑制し、このバランスがアナフィラキシーの強さを決めると考えられます。
用語解説
*1 CD300: 細胞外領域の相同性が高い免疫受容体群であり、機能的に活性化型(CD300d3など)と抑制型(CD300fなど)に分けられる。
*2 スフィンゴミエリン(SM)やセラミド: 生体内に存在する脂質であり、さまざまな種類(炭素数の違いや二重結合の有無など)が存在する。
*3 高親和性IgE受容体(FcεRI): α鎖とβ鎖、γ鎖の2量体で形成(αβγ2)され、マスト細胞表面に発現する。IgEはα鎖に結合する。β鎖とγ鎖は細胞内領域に活性化シグナルの伝達モチーフ(ITAM)をもつ。FcεRIがIgEと抗原により架橋刺激されると、β鎖とγ鎖のITAMがリン酸化を受けてFcεRIシグナルが起動する。
*4 アナフィラキシー: FcεRIシグナルを介するマスト細胞の活性化(脱顆粒)により引き起こされる即時型アレルギーの重症型であり、皮膚・消化器・呼吸器など全身の症状を伴う。
*5 CD300d3: (細胞内領域にITAMをもつ)γ鎖の2量体と会合して、活性化シグナルを伝える。
*6 CD300f: 細胞内領域に抑制シグナルの伝達モチーフ(ITIMやITSM)をもち、ITIMやITSMのリン酸化を介して抑制シグナルを伝える。
*7 受動的皮膚アナフィラキシー(PCA): IgEと抗原による皮膚マスト細胞の脱顆粒に伴う皮膚アナフィラキシーを評価(血管透過性を指標として)するマウスモデル。具体的には、マウスの耳介にIgEを皮下注射した翌日、抗原と青色色素を静脈注射し、その30分後の耳介に漏出する色素量を定量化する。
研究者のコメント
マウスモデルの解析から、マスト細胞の周囲に存在する脂質のセラミドやスフィンゴミエリンを識別する免疫受容体が高親和性IgE受容体シグナルを制御し、アナフィラキシーの強さを決めることがわかりました。今後も、マスト細胞の活性化(脱顆粒)を促進あるいは抑制する生体内の仕組みの解明を目指し、その成果をアレルギー疾患の予防・治療法開発につなげたいと思います。
原著論文
本研究はCell Reports誌のオンライン版に2026年3月4日付で公開されました。
タイトル: IgE-dependent anaphylaxis is regulated by sphingolipid binding to activating and inhibitory CD300 family members.
タイトル(日本語訳): IgE依存的なアナフィラキシーはスフィンゴ脂質と活性化型および抑制型のCD300ファミリー分子との結合によって制御される
著者: Kumi Izawa1), Ayako Kaitani1), Yutaka Enomoto2,3), Tomoaki Ando1), Yuka Yasuda4), Tomoaki Kahyo5,6), Akie Maehara1), Risa Yamamoto1), Natsumi Uchida1), Yuka Furuichi1), Kaiyan Wei1), Hiromichi Yamada1,7), Yu Kawasumi1,8), Takuma Ide1,8), Masahiro Nakamura8), Shino Uchida1,9), Nobuhiro Nakano1), Junko Ishikawa4), Hiroshi Kiyonari10), Takaya Abe10), Toshiaki Shimizu1,7), Toshio Kitamura2,3,11), Hideoki Ogawa1), Ko Okumura1), Mitsutoshi Setou5,12), Jiro Kitaura1,13)
著者(日本語表記): 伊沢久未1)、貝谷綾子1)、榎本豊2,3)、安藤智暁1)、安田由夏4)、華表友暁5,6)、前原明絵1)、山本里彩1)、内田菜摘1)、古市優果1)、魏恺彦 1)、山田啓迪1,7)、川角佑1.8)、井出拓磨1,8)、中村真浩8)、内田志野1,9)、中野信浩1)、石川准子4)、清成寛10)、阿部高也10)、清水俊明1,7)、北村俊雄2,3,11)、小川秀興1)、奥村康1)、瀬藤光利5,12)、北浦次郎1,13)
著者所属: 1) 順天堂大学 大学院医学研究科アトピー疾患研究センター、2)東京大学 医科学研究所細胞療法、3)東京大学 大学院薬学系研究科・薬学部分子腫瘍学、4)花王株式会社、5)浜松医科大学 細胞分子解剖学、6) 浜松医科大学 光医学総合研究所国際マスイメージングセンター/光量子技術開発部門量子イメージング研究、7) 順天堂大学 大学院医学研究科小児思春期発達・病態学、8) 順天堂大学 大学院医学研究科耳鼻咽喉・頭頸科学、9) 順天堂大学 医学部内科学教室・消化器内科学講座、10)国立研究開発法人 理化学研究所生体モデル開発チーム、11)公益財団法人神戸医療産業都市推進機構、12)浜松医科大学 国際マスイメージングセンター、13) 順天堂大学 大学院医学研究科アレルギー・炎症制御学
DOI: https://doi.org/10.1016/j.celrep.2026.117054
本研究はJSPS科研費JP26293231, JP17H04217, JP20H03721, JP23H02946、公益財団法人武田科学振興財団、公益財団法人持田記念医学薬学振興財団などの支援を受け多施設との共同研究の基に実施されました。
なお、本研究にご協力いただいた皆様には深謝いたします。
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
