心臓サルコイドーシスにおける心筋生検陽性患者の特徴、予測因子と予後
― 世界最大級の心臓サルコイドーシスレジストリからの報告 ―
順天堂大学大学院医学研究科循環器内科学の前田大智 非常勤助教、藤本雄大 大学院生、末永祐哉 准教授らの研究グループは、心臓サルコイドーシスにおける心筋生検陽性患者の特徴、予測因子と予後を検証しました。心臓サルコイドーシスの診断において、心筋生検は特異度の高い重要な検査ですが、侵襲(体への負担)を伴ううえ感度が十分高くないことが課題でした。どのような患者で心筋生検が陽性になりやすいかについては、これまで主としてフィンランドの単一コホートからの報告に限られていました。本研究は、世界最大規模の多施設レジストリデータ*1である ILLUMINATE-CS を用いて、日本人心臓サルコイドーシス患者において、心室中隔基部壁厚、18F-FDG PET*2陽性セグメント数、B型ナトリウム利尿ペプチド(BNP)*3値が心筋生検陽性を予測する因子であることを明らかにしました。本成果は、心臓サルコイドーシス診断において、より適切な患者選択のもとで安全かつ効率的に心筋生検を行うための一助となる重要な報告と考えられます。本論文はJournal of Cardiac Failure誌のオンライン版に2026年5月12日付で公開されました。
本研究成果のポイント
● 日本の心臓サルコイドーシスレジストリを用いて、心筋生検陽性例の頻度と特徴を明らかにした
● フィンランドのレジストリで報告された心筋生検陽性の予測因子が、日本人コホートでも一定程度支持された
● 心エコー図、PET検査、BNPといった日常診療で得られる指標から、心筋生検陽性となりやすい患者像が示された
背景
サルコイドーシスは、全身のさまざまな臓器に非乾酪性類上皮細胞肉芽腫を形成する炎症性疾患です。心臓に病変を認める場合は心臓サルコイドーシスと呼ばれ、房室ブロック、心室頻拍・心室細動などの重篤な不整脈や心不全、突然死の原因となることが知られています。
心臓サルコイドーシスの診断では、心筋生検によって心筋内に肉芽腫を証明できれば特異性の高い確定診断が可能ですが、病変がまだらに分布するため、心筋生検を行っても診断に至らないことが少なくありません。また、心筋生検は侵襲的手技であるため、どの患者に実施すべきかを適切に判断することが重要です。
これまで、心筋生検陽性を予測する因子については海外からの限られた報告があるのみで、日本人を含む独立した大規模コホートでの検証は十分ではありませんでした。そこで本研究では、日本の多施設レジストリである ILLUMINATE-CS を用いて、心臓サルコイドーシス患者における心筋生検陽性の頻度、関連する臨床的特徴、予後を包括的に検討しました。
内容
本研究では、ILLUMINATE-CS レジストリに登録された心臓サルコイドーシス患者のうち、診断時に心筋生検を受けた 246人のデータを統計学的に解析しました。対象患者の平均年齢は 61.0歳、男性は 42.3% でした。
その結果、55人(22.2%)で心筋生検陽性所見が認められました。まず、既報のフィンランドコホート(MIDFIN)で提唱されていた予測因子(心室頻拍・心室細動の既往、左室駆出率45%以下、心筋トロポニン高値、心室中隔の中部から心尖部にかけての心臓MRI遅延造影)について、日本人コホートでも検証したところ、症例数は限られるものの、心筋生検陽性率はスコア上昇に伴って増加し、方向性の一貫した関連が確認されました。
さらに ILLUMINATE-CS 全体で心筋生検陽性に関連する因子を検討したところ、①心室中隔基部壁厚が厚いこと、②18F-FDG PETで陽性となるセグメント数が多いこと、③BNP値が高いこと、の3項目が独立した予測因子として抽出されました。各因子の至適カットオフ値は、心室中隔基部壁厚 8.9 mm、18F-FDG PET陽性セグメント数 10、BNP 155.0 pg/mL でした。これら3項目のうち該当する項目数が多いほど、心筋生検陽性率は高くなりました。
一方で、中央値 2.9年間の追跡期間中における主要評価項目(全死亡、心不全入院、致死性心室性不整脈イベントの複合)については、心筋生検陽性群と陰性群との間で統計学的な有意差は認められませんでした。
以上の結果より、心臓サルコイドーシスにおいては、病変の活動性や広がり、心筋障害の程度を反映する所見が、心筋生検陽性と関連する可能性(図1)が示されました。
今後の展開
今回の研究により、心臓サルコイドーシス患者において、心室中隔基部壁厚、18F-FDG PET所見、BNP値といった日常診療で比較的評価しやすい指標から、心筋生検陽性となる可能性を推定できることが示されました。これは、侵襲的な心筋生検をより適切な患者に絞って実施するうえで有用であると考えられます。
ただし、本研究で示された予測モデルは日本人コホート内で作成された探索的なものであり、今後はより大規模な独立コホートや国際共同研究による検証が必要です。将来的には、こうした知見をもとに、心臓サルコイドーシスのより正確で効率的な診断アルゴリズムの構築が進むことが期待されます。
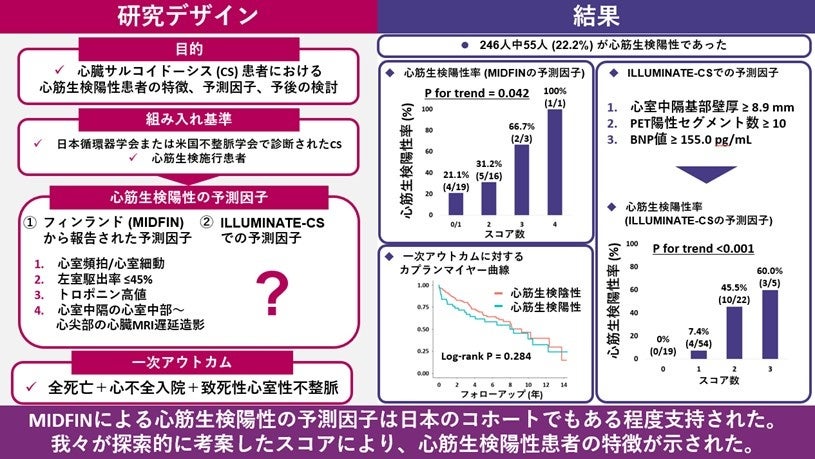
本研究では、心臓サルコイドーシスにおける心筋生検陽性例の特徴と予測因子を検討した。本研究は、①MIDFINで報告された予測因子が日本人でも適用可能か確認する、②ILLUMINATE-CSコホート内での日本人における予測因子を探索すること、の2つを目的とした。あわせて、心筋生検陽性の有無による予後の違いも比較した。心筋生検を受けた246人のうち、22.2%で陽性であった。MIDFIN由来の予測因子は、ILLUMINATE-CSコホートにおいても方向性の一貫した関連を示した(傾向性のP=0.042)。また、ILLUMINATE-CSコホートでは、心室中隔基部壁厚、18F-FDG PET陽性のセグメント数、BNP値が心筋生検陽性の予測因子として抽出され、これらを満たす数が多いほど陽性率も高くなった(傾向性のP<0.001)。一方で、心筋生検陽性群と陰性群との間で予後に有意な差は認められなかった。
用語解説
*1 多施設レジストリデータ:特定の疾患に関する様々なデータ(患者数、検査結果、予後など)を調査するため、複数の病院において、特定の疾患に罹患した患者を網羅的に登録したデータのことです。
*2 18F-FDG PET:ブドウ糖に似た性質を持つ放射性薬剤(18F-FDG)を体内に投与し、その取り込みを画像として調べる検査です。炎症の強い部分ではこの薬剤が集まりやすいため、心臓サルコイドーシスなどで心筋の炎症の広がりや活動性を評価するのに役立ちます。
*3 BNP(B型ナトリウム利尿ペプチド):主に心臓に負担がかかったときに分泌される物質で、血液検査で測定されます。心不全の重症度や心臓への負担の程度を知るために広く用いられます。
研究者のコメント
心臓サルコイドーシス自体はまれな病気ではありますが、日本人に多いことが知られており、その診断・治療の進歩は非常に重要です。技術の発展とともに、画像診断の精度が向上しておりますが、やはり実際の心臓の筋肉から心臓サルコイドーシスを証明する以上に確実性の高い診断方法はありません。心筋生検は多くの場合は安全に施行可能ですが、侵襲性のある検査のため、本研究が安全かつ正確な心臓サルコイドーシスの診断の一助になりましたら幸いです。
原著論文
本研究はJournal of Cardiac Failure誌のオンライン版に2026年5月12日付で公開されました。
タイトル: Positive Endomyocardial Biopsy in Cardiac Sarcoidosis: Predictors and Outcomes From the Japanese ILLUMINATE-CS (Illustration of the Management and prognosis of JapaNese PATiEnts with Cardiac Sarcoidosis) Registry
タイトル(日本語訳): 心臓サルコイドーシスにおける心筋生検陽性の予測因子とその予後(日本のILLUMINATE-CSレジストリからの報告)
著者:Daichi Maeda 1.2), Yudai Fujimoto 1), Takeru Nabeta 3), Takeshi Kitai 4), Yoshihisa Naruse 5), Tatsunori Taniguchi 6), Hidekazu Tanaka 7), Ryota Morimoto 8), Yuichi Baba 9), Kenji Yoshioka 10), and Yuya Matsue 1)
著者(日本語表記): 前田 大智 1.2), 藤本 雄大 1), 鍋田 健 3), 北井 豪 4), 成瀬 代士久 5) , 谷口 達典 6), 田中 秀和 7), 森本 竜太 8), 馬場 裕一 9), 吉岡 賢二 10), 末永 祐哉 1)
著者所属:1) Department of Cardiovascular Biology and Medicine, Juntendo University Graduate School of Medicine, Tokyo, Japan 2)Department of Cardiology, Osaka Medical and Pharmaceutical University, Takatsuki, Japan 3) Department of Cardiovascular Medicine, Kitasato University School of Medicine, Sagamihara, Japan 4) Department of Cardiovascular Medicine, National Cerebral and Cardiovascular Center, Suita, Japan 5) Division of Cardiology, Internal Medicine Ⅲ, Hamamatsu University School of Medicine, Hamamatsu, Japan 6) Department of Cardiovascular Medicine, Osaka University Graduate School of Medicine, Suita, Japan 7) Division of Cardiovascular Medicine, Department of Internal Medicine, Kobe University Graduate School of Medicine, Kobe, Japan 8) Department of Cardiology, Nagoya University Graduate School of Medicine, Nagoya, Japan 9) Department of Cardiology and Geriatrics, Kochi Medical School, Kochi University, Nankoku, Japan 10) Department of Cardiology, Kameda Medical Center, Kamogawa, Japan
著者所属(日本語表記): 1) 順天堂大学 大学院医学研究科 循環器内科学 2) 大阪医科薬科大学 循環器内科 3) 北里大学 循環器内科学 4) 国立循環器病研究センター 心臓血管内科 5) 浜松医科大学 内科学第三講座 6) 大阪大学 大学院医学系研究科 循環器内科学 7) 神戸大学 大学院医学研究科 循環器内科学 8) 名古屋大学 大学院医学系研究科 循環器内科学 9) 高知大学 老年病・循環器内科学 10)亀田総合病院 循環器内科
DOI: 10.1016/j.cardfail.2026.02.025
本研究はJSPS科研費22K16152,および国立研究開発法人日本医療研究開発機構 (AMED) JP25ek0109795の支援を受け多施設との共同研究の基に実施されました。なお、本研究にご協力いただいた皆様には深謝いたします。
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
