体内の有害な活性硫黄を無毒化・排出する二重制御機構を解明―メチル化と酸化による“二重制御”が生体を防御する仕組み―
千葉大学大学院薬学研究院の福本泰典講師および小椋康光教授らの研究グループは、群馬大学および東邦大学との共同研究により、生体内で生成される活性硫黄種 (RSS)(注1)がメチル化によって無毒化され、尿として体外へ排出される機構を明らかにしました。本研究は、RSSがメチル化と酸化という2つの異なる経路で制御されることを示しており、生体内の還元ストレスに関わる制御機構の理解を深める基盤となります。今後、RSSの制御破綻と生理的・病理的変化や疾患との関連の解明に寄与することが期待されます。
本研究成果は、2026年4月1日に、学術誌Redox Biologyで公開されました。
(論文はこちら:10.1016/j.redox.2026.104144)
■研究の背景
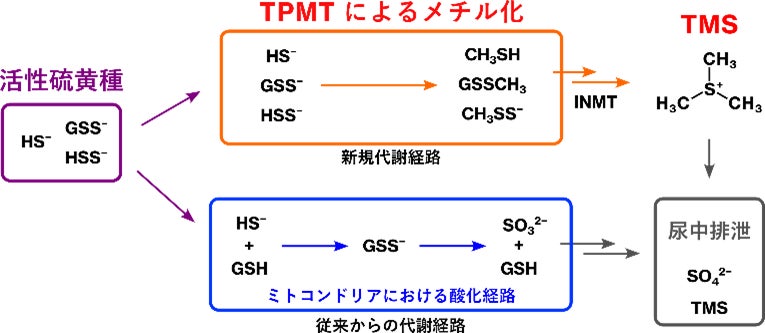
RSSは生命維持に不可欠である一方、過剰蓄積は細胞毒性を招くため、生体内ではその濃度が調節されています。これまでRSSの消失は、主にミトコンドリア内の酵素による酸化経路が担うと考えられてきました。大量のRSS蓄積や還元ストレス下など酸化系が正常に機能しない条件下では、安全な形で無毒化・排出する仕組みが存在すると考えられてきましたが、その分子機構は未解明でした。
■研究成果のポイント
1. 体内で有害となりうるRSSを無毒化し、尿中へ排出する「三段階メチル化経路」の仕組みを解明
メチル化酵素に着目し生化学的解析を行った結果、RSSがTPMT(注2)によりメチル化されることを初めて特定しました。この反応を起点として、INMT(注3)などの酵素の働きにより、反応性の高いRSSは揮発性・毒性の低いTMS(注4)へと三段階で変換され、最終的に尿として体外へ排出される代謝経路が存在することが明らかになりました。TMSはヒトの尿中に検出される硫黄代謝物として知られていましたが、本研究によりその生成機構が解明されました。
2. 「メチル化」経路と「酸化」経路による“二重制御”を発見
RSSはミトコンドリアの「酸化」酵素によって代謝されることが知られていましたが、本研究によりこれとは別にメチル化という異なる経路も並行して存在することが示されました。これら2経路は単なる冗長な仕組みではなく、状況に応じてセーフガードとして働く “二重制御機構”であることが示唆されました。
3. 計算科学的解析により活性硫黄のメチル化における基質選択性の分子機構を解明
in silico(計算科学的)解析と生化学実験により、TPMTが特定のRSSを優先的にメチル化する分子機構を解明した結果、メチル化効率は分子の電気的性質よりも、酵素活性部位における「立体障害」の少なさに強く依存していることが判明し、どのRSSが選択的に無毒化・排出されるかの仕組みが示されました。
■今後の展望(研究者コメント)
本研究により、未解明だった活性硫黄の無毒化と排出の仕組みが明らかとなりました。本研究で示した二重制御は、生体内における反応選択性と代謝制御の基本原理を示すものです。この成果は、基礎生物学的な重要性に留まらず、医療への貢献も期待されます。例えば、遺伝的な個人差(多型)が激しいTPMTの活性が低い人におけるRSS過剰蓄積による健康リスクを考慮した個別化医療や、RSSを放出する薬剤の効果を高めたり、副作用を減らしたりすることで、より安全で適切な治療の実現が期待されます。今後は、TPMT欠損モデルにおいてRSSの過剰蓄積と制御の破綻がどのような生理的・病理的変化につながるのかを明らかにしていきたいと考えています。
■用語解説
注1)活性硫黄種(Reactive Sulfur Species: RSS):生体内で生成される硫黄を含む反応性の高い分子群の総称。生体防御や細胞間のシグナル伝達に関与する一方で、過剰に蓄積すると細胞に傷害を引き起こす。
注2)TPMT(チオプリンS-メチルトランスフェラーゼ):生体内でメチル化反応を担う酵素の一つ。本研究では、活性硫黄の無毒化と排出に関与する酵素として新たに位置づけられた。
注3)INMT(インドールエチルアミンN-メチルトランスフェラーゼ):生体内でメチル化反応を担う酵素の一つであり、特定の低分子化合物の代謝に関与する。
注4)TMS(トリメチルスルホニウム): 尿中に検出される硫黄化合物。本研究により、活性硫黄が多段階のメチル化を受けることで生成される最終産物であることが証明された。
■論文情報
タイトル:Reactive sulfur species are inactivated and excreted as trimethylsulfonium ion by thiopurine S-methyltransferase
著 者:Yasunori Fukumoto, Momoka Uchida, Yoshikazu Yamagishi, Natsu Saito, Ayune Watanabe, Rina Mukasa, Ryosuke Kobayashi, Takuro Horii, Izuho Hatada, Yu-Ki Tanaka, Noriyuki Suzuki, Yasumitsu Ogra
雑誌名:Redox Biology
DOI: 10.1016/j.redox.2026.104144
■研究プロジェクトについて
本研究は科学研究費助成事業 (24K09793, 24H00749, 24K21304, 25K02898, 22K05345)、およびアジレントテクノロジーズ社のACT-UR プログラム (#4366, #4489) による支援を受けて行われました
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
