<幹細胞治療のテラとセネジェニックス研究所による共同事業> 国内初、新型コロナウィルス感染症に対する幹細胞治療 臨床試験を開始
レムデシビルやアビガンでは抑制困難なサイトカインストームに有効とされる幹細胞治療で重症化防ぐ
先端医療支援事業を手掛けるCENEGENICS JAPAN 株式会社(本社:東京都中央区、代表取締役社長:藤森徹也 以下「セネジェニックス・ジャパン」)と幹細胞治療の研究開発を行うテラ株式会社(本社:東京都新宿区、代表取締役社長:平智之 以下「テラ」)は共同で、2020年5月14日から開始した新型コロナウィルス感染症(COVID-19)に対する幹細胞治療法開発に向けたメキシコでの臨床研究において、感染患者1人の症状回復を確認し、国内企業として初めて新型コロナウイルス感染症に対する幹細胞治療の臨床試験に成功したことをお知らせいたします。
2020年5月13日から、セネジェニックス・ジャパンが提携関係を有するCENEGENICS Mexico Inc.(以下「セネジェニックス・メキシコ」)が保有し、メキシコ国内で承認を得ている米国FDAの基準を満たした臍帯由来幹細胞(UC-MSC)を用いて、コロナウィルス感染症により中等度以上の呼吸器症状が出現している新型コロナ肺炎患者(18歳~75歳)総計75名を対象に、臨床研究を行っております。第一例目の投与がなされて以来、5月26日までの時点で重度のCOVID-19肺炎患者として登録された症例数は9例であり、引き続き50症例まで登録数を増やすことを目指し、治療を続けてまいります。判定には2週間以上の経過観察が必要なため、現段階では効果判定に至った症例はなく、治療が続いている状況ですが第一例目の患者は、肺炎と呼吸機能の改善が認められ、引き続き経過観察中です。(人工呼吸器をつけた重症患者が、投与後3日後には、人工呼吸器を外すほど回復しました。)治療プロトコル及び臨床研究の成果を、セネジェニックスジャパンを介してテラ株式会社に提供し、引き続き幹細胞を使った治療法の確立を目指してまいります。研究成果は、同年7月に発表予定です。
さらに、臍帯由来幹細胞での臨床研究に追加して、成人ヒト経血から得ることができる幹細胞であり、原材料が胎盤や臍帯と比較して入手しやすいとされる「子宮内膜由来幹細胞(MenSCs)※1」治療における臨床研究を開始しました。対象者は、臍帯由来幹細胞治療と同様に、COVID-19によって重症化した患者に対して行い、目標症例は30症例を予定しており、標準治療を行う比較対象群は、15症例を予定しています。2020年5月26日(メキシコ時間25日)時点で、COVID-19の悪化で人工呼吸器に依存する重度のCOVID-19肺炎患者10症例が登録され二重盲検法により子宮内膜由来幹細胞が投与され、副作用および治療効果を観察しています。臍帯由来幹細胞治療と同様、2020年9月に終了予定です。
我々は、COVID-19に対して免疫を調節する臍帯由来幹細胞および子宮内膜由来幹細胞を利用した治療法の開発に貢献し、倫理的に問題が少ない、副作用の少ない治療法を提供する事で、患者の皆様への貢献と、企業価値の向上を実現してまいります。
※1 MenSCs(子宮内膜由来幹細胞)
臍帯由来幹細胞は受精卵でなく臍帯から取得することができるため倫理的問題が少ないとして再生医療分野での応用が期待されている一方で、原材料に臍帯が必要であることから供給に課題があります。子宮内膜由来幹細胞は、臍帯由来幹細胞と同じく安全で倫理的問題が少ないだけでなく、経血から作製することができるため、臍帯等と比べ原材料の供給が容易です。また、子宮内膜由来幹細胞も臍帯由来幹細胞と同様に、腫瘍壊死因子-a(TNF-a)、インターフェロン-g、インターロイキン(IL)-6と呼ばれる炎症性因子の発現を抑制し、インターロイキン(IL)-4と呼ばれる因子の分泌を促進し、制御性T細胞やM2マクロファージの数を増加させることで、免疫調節、特に免疫抑制の役割を発揮するなどの利点を持った幹細胞です※2,※3。
※2 2007 Human Reproduction Update, Vol.13、No.1: 87-101. Gargett C. E. et al.
※3 2017 Stem Cell Research & Therapy 8:9. Chen et al.
【間葉系幹細胞での治療について】
現在、新型コロナウィルス感染症(COVID-19)に対する有効な治療薬の開発は人類共通の喫緊の課題となっています。入院した患者のうち 31~67%の割合で ※1急性呼吸窮迫症候群(以下、「ARDS」)を発症しており、死亡例では ARDSとの合併症が 81~93%の割合で確認されており、ARDSを治療する必要性が高いと考えられています。そのARDSの治療のために、その炎症を抑え、組織再生する能力のある ※2間葉系幹細胞(以下、「MSCs」)に対する研究が現在世界中で行われています。この度開始する臨床研究で使用する幹細胞は、へその緒などから採取できる臍帯由来のものであるため、事前に準備しておくことができ、骨髄や脂肪から採取する幹細胞に比べ原材料の入手にも比較的余裕があります。そのため、患者への安定的かつ迅速な対応が期待できます。
※1<ARDS(急性呼吸窮迫症候群)>
ARDS とは、炎症により肺が損傷を受け重度の呼吸不全となる症状のことですが、中国の武漢で始まった新型コロナウイルス感染症(COVID-19)は、この ARDS を引き起すことが確認されています。ARDS を引き起こす原因が、ウイルスによる直接の損傷なのか、免疫系の過剰反応による損傷なのかは正確にはわかっていませんが、COVID-19 による重症例の多くの患者さんがARDS を発症していることから、COVID-19 の重症化を避けるために はARDS の治療法の開発が必要と考えられています。
※2<MSCs(間葉系幹細胞)>
様々な人間の部位に変化する前の 1 番最初の細胞を幹細胞と言いますが、かつては受精卵から取得されることが多く、欧米では倫理的に問題視されることがありました。しかし、幹細胞の中でも MSCs(間葉系幹細胞)は、自分の骨髄、脂肪組織、胎盤、臍帯、歯髄等から取得することができるため、このような批判を回避することができます。MSCs は、自分の身体から取得するため、投与時の安全性が高く、倫理的問題が少ないと考えら れ、再生医療分野での応用が期待されている幹細胞です。このため再生医療分野で、骨、血管、心筋等の再構 築に利用する研究が進められている一方で、免疫反応を抑制する効果も証明されており、ARDS の治療への適用も期待されています。
【メキシコでの臨床研究について】
※写真はメキシコ病院施設の様子
研究特徴について:
(臍帯由来幹細胞及び子宮内膜由来幹細胞)
① 対象患者は、PCR検査で陽性と判断され、酸素飽和度92%以下となった重度患者が対象。
② メキシコ内で3つの研究施設を利用して実施。
患者への投与について:
① 既にメキシコで承認を取得している幹細胞を使用するため、迅速に臨床研究に入ることができる。
② 他家細胞(他人の細胞)を培養したものを使うため、今後治療が必要な方へ時間を置かずに治療を行うことができる。
③ 患者1人につき、約1億5000万個の臍帯由来幹細胞を点滴静注で投与する。
【今後のスケジュール】
5月13日 メキシコにて、臨床研究を開始
5月27日 臨床研究の中間報告
7月中 メキシコでの臨床研究終了、結果報告
変更となる可能性もございますが、今秋中の国内治験開始、新薬承認を目指しております。
※情報更新があり次第、随時プレスリリースなどでご案内申し上げます。
【国際新型コロナウイルス細胞治療研究会】(https://iact4c.org/)
新型コロナウイルスに対する、幹細胞治療の有効性を確認し、世界の各研究機関と連携して研究成果をより発展していくための団体「国際新型コロナウイルス細胞治療研究会」が発足しました。コロナウイルスに対して、様々な研究が進む学術交流の場として期待しております。セネジェニックス・ジャパンがその運営事務局を務めております。本研究会にて、新型コロナウイルスに対していかに幹細胞治療が有効的か、分かりやすく解説する動画を作成いたしました。
【UAE(アラブ首長国連邦)での幹細胞治療研究事例】
世界各国において新型コロナウイルスに対する様々な研究が進んでいますが、幹細胞治療の観点からすでに成果が生まれました。
UAEの研究施設「アブダビ幹細胞センター」は5月1日に、幹細胞治療によって73名のコロナ患者を回復させたと発表しました。患者から採取した自身の血液の幹細胞を活性化させ、細かい霧状にして吸入させたところ、肺の細胞が再生し、全員が完治して副作用もなかったとのことです。すでに臨床試験の第1段階を通過していて、有効性を実証するための試験が今後行われる予定です。UAE以外にも、アメリカFDAや中国科学技術部にて治験が認められています。
【会社概要】
会社名 :テラ 株式会社
所在地 :東京都中央区銀座2丁目5-4 ファサード銀座3階
資本金 :27億2200万円
代表取締役:平 智之
事業内容 :医療機関に対する樹状細胞ワクチン療法等、細胞医療に関する技術・運用ノウハウの提供
樹状細胞ワクチン療法等、再生・細胞医療に関する研究開発
URL :https://www.tella.jp/
会社名 :CENEGENICS JAPAN 株式会社
所在地 :東京都中央区銀座2丁目5-4 ファサード銀座3階
資本金 :1億9000万円
代表取締役:藤森 徹也
事業内容 :遺伝子・細胞・組織等を用いた先端医療支援事業等
URL :https://cenegenics-japan.com/
2020年5月13日から、セネジェニックス・ジャパンが提携関係を有するCENEGENICS Mexico Inc.(以下「セネジェニックス・メキシコ」)が保有し、メキシコ国内で承認を得ている米国FDAの基準を満たした臍帯由来幹細胞(UC-MSC)を用いて、コロナウィルス感染症により中等度以上の呼吸器症状が出現している新型コロナ肺炎患者(18歳~75歳)総計75名を対象に、臨床研究を行っております。第一例目の投与がなされて以来、5月26日までの時点で重度のCOVID-19肺炎患者として登録された症例数は9例であり、引き続き50症例まで登録数を増やすことを目指し、治療を続けてまいります。判定には2週間以上の経過観察が必要なため、現段階では効果判定に至った症例はなく、治療が続いている状況ですが第一例目の患者は、肺炎と呼吸機能の改善が認められ、引き続き経過観察中です。(人工呼吸器をつけた重症患者が、投与後3日後には、人工呼吸器を外すほど回復しました。)治療プロトコル及び臨床研究の成果を、セネジェニックスジャパンを介してテラ株式会社に提供し、引き続き幹細胞を使った治療法の確立を目指してまいります。研究成果は、同年7月に発表予定です。
さらに、臍帯由来幹細胞での臨床研究に追加して、成人ヒト経血から得ることができる幹細胞であり、原材料が胎盤や臍帯と比較して入手しやすいとされる「子宮内膜由来幹細胞(MenSCs)※1」治療における臨床研究を開始しました。対象者は、臍帯由来幹細胞治療と同様に、COVID-19によって重症化した患者に対して行い、目標症例は30症例を予定しており、標準治療を行う比較対象群は、15症例を予定しています。2020年5月26日(メキシコ時間25日)時点で、COVID-19の悪化で人工呼吸器に依存する重度のCOVID-19肺炎患者10症例が登録され二重盲検法により子宮内膜由来幹細胞が投与され、副作用および治療効果を観察しています。臍帯由来幹細胞治療と同様、2020年9月に終了予定です。
我々は、COVID-19に対して免疫を調節する臍帯由来幹細胞および子宮内膜由来幹細胞を利用した治療法の開発に貢献し、倫理的に問題が少ない、副作用の少ない治療法を提供する事で、患者の皆様への貢献と、企業価値の向上を実現してまいります。
※1 MenSCs(子宮内膜由来幹細胞)
臍帯由来幹細胞は受精卵でなく臍帯から取得することができるため倫理的問題が少ないとして再生医療分野での応用が期待されている一方で、原材料に臍帯が必要であることから供給に課題があります。子宮内膜由来幹細胞は、臍帯由来幹細胞と同じく安全で倫理的問題が少ないだけでなく、経血から作製することができるため、臍帯等と比べ原材料の供給が容易です。また、子宮内膜由来幹細胞も臍帯由来幹細胞と同様に、腫瘍壊死因子-a(TNF-a)、インターフェロン-g、インターロイキン(IL)-6と呼ばれる炎症性因子の発現を抑制し、インターロイキン(IL)-4と呼ばれる因子の分泌を促進し、制御性T細胞やM2マクロファージの数を増加させることで、免疫調節、特に免疫抑制の役割を発揮するなどの利点を持った幹細胞です※2,※3。
※2 2007 Human Reproduction Update, Vol.13、No.1: 87-101. Gargett C. E. et al.
※3 2017 Stem Cell Research & Therapy 8:9. Chen et al.
【間葉系幹細胞での治療について】
現在、新型コロナウィルス感染症(COVID-19)に対する有効な治療薬の開発は人類共通の喫緊の課題となっています。入院した患者のうち 31~67%の割合で ※1急性呼吸窮迫症候群(以下、「ARDS」)を発症しており、死亡例では ARDSとの合併症が 81~93%の割合で確認されており、ARDSを治療する必要性が高いと考えられています。そのARDSの治療のために、その炎症を抑え、組織再生する能力のある ※2間葉系幹細胞(以下、「MSCs」)に対する研究が現在世界中で行われています。この度開始する臨床研究で使用する幹細胞は、へその緒などから採取できる臍帯由来のものであるため、事前に準備しておくことができ、骨髄や脂肪から採取する幹細胞に比べ原材料の入手にも比較的余裕があります。そのため、患者への安定的かつ迅速な対応が期待できます。
※1<ARDS(急性呼吸窮迫症候群)>
ARDS とは、炎症により肺が損傷を受け重度の呼吸不全となる症状のことですが、中国の武漢で始まった新型コロナウイルス感染症(COVID-19)は、この ARDS を引き起すことが確認されています。ARDS を引き起こす原因が、ウイルスによる直接の損傷なのか、免疫系の過剰反応による損傷なのかは正確にはわかっていませんが、COVID-19 による重症例の多くの患者さんがARDS を発症していることから、COVID-19 の重症化を避けるために はARDS の治療法の開発が必要と考えられています。
※2<MSCs(間葉系幹細胞)>
様々な人間の部位に変化する前の 1 番最初の細胞を幹細胞と言いますが、かつては受精卵から取得されることが多く、欧米では倫理的に問題視されることがありました。しかし、幹細胞の中でも MSCs(間葉系幹細胞)は、自分の骨髄、脂肪組織、胎盤、臍帯、歯髄等から取得することができるため、このような批判を回避することができます。MSCs は、自分の身体から取得するため、投与時の安全性が高く、倫理的問題が少ないと考えら れ、再生医療分野での応用が期待されている幹細胞です。このため再生医療分野で、骨、血管、心筋等の再構 築に利用する研究が進められている一方で、免疫反応を抑制する効果も証明されており、ARDS の治療への適用も期待されています。
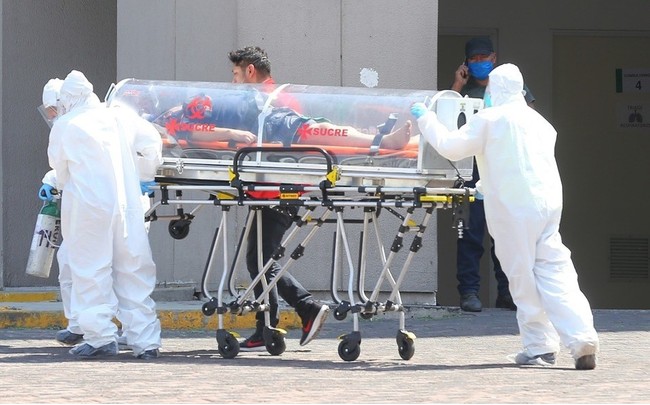
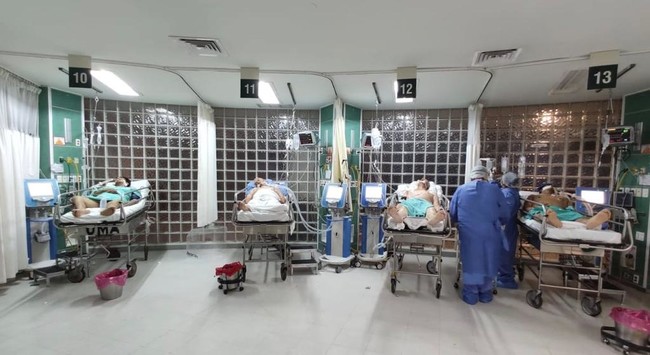
【メキシコでの臨床研究について】
※写真はメキシコ病院施設の様子
研究特徴について:
(臍帯由来幹細胞及び子宮内膜由来幹細胞)
① 対象患者は、PCR検査で陽性と判断され、酸素飽和度92%以下となった重度患者が対象。
② メキシコ内で3つの研究施設を利用して実施。
患者への投与について:
① 既にメキシコで承認を取得している幹細胞を使用するため、迅速に臨床研究に入ることができる。
② 他家細胞(他人の細胞)を培養したものを使うため、今後治療が必要な方へ時間を置かずに治療を行うことができる。
③ 患者1人につき、約1億5000万個の臍帯由来幹細胞を点滴静注で投与する。
【今後のスケジュール】
5月13日 メキシコにて、臨床研究を開始
5月27日 臨床研究の中間報告
7月中 メキシコでの臨床研究終了、結果報告
変更となる可能性もございますが、今秋中の国内治験開始、新薬承認を目指しております。
※情報更新があり次第、随時プレスリリースなどでご案内申し上げます。
【国際新型コロナウイルス細胞治療研究会】(https://iact4c.org/)
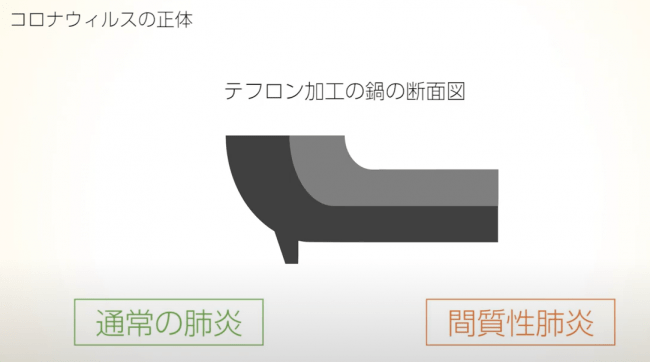
新型コロナウイルスに対する、幹細胞治療の有効性を確認し、世界の各研究機関と連携して研究成果をより発展していくための団体「国際新型コロナウイルス細胞治療研究会」が発足しました。コロナウイルスに対して、様々な研究が進む学術交流の場として期待しております。セネジェニックス・ジャパンがその運営事務局を務めております。本研究会にて、新型コロナウイルスに対していかに幹細胞治療が有効的か、分かりやすく解説する動画を作成いたしました。
【UAE(アラブ首長国連邦)での幹細胞治療研究事例】
世界各国において新型コロナウイルスに対する様々な研究が進んでいますが、幹細胞治療の観点からすでに成果が生まれました。
UAEの研究施設「アブダビ幹細胞センター」は5月1日に、幹細胞治療によって73名のコロナ患者を回復させたと発表しました。患者から採取した自身の血液の幹細胞を活性化させ、細かい霧状にして吸入させたところ、肺の細胞が再生し、全員が完治して副作用もなかったとのことです。すでに臨床試験の第1段階を通過していて、有効性を実証するための試験が今後行われる予定です。UAE以外にも、アメリカFDAや中国科学技術部にて治験が認められています。
【会社概要】
会社名 :テラ 株式会社
所在地 :東京都中央区銀座2丁目5-4 ファサード銀座3階
資本金 :27億2200万円
代表取締役:平 智之
事業内容 :医療機関に対する樹状細胞ワクチン療法等、細胞医療に関する技術・運用ノウハウの提供
樹状細胞ワクチン療法等、再生・細胞医療に関する研究開発
URL :https://www.tella.jp/
会社名 :CENEGENICS JAPAN 株式会社
所在地 :東京都中央区銀座2丁目5-4 ファサード銀座3階
資本金 :1億9000万円
代表取締役:藤森 徹也
事業内容 :遺伝子・細胞・組織等を用いた先端医療支援事業等
URL :https://cenegenics-japan.com/
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザーログイン既に登録済みの方はこちら
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
- 種類
- その他
- ダウンロード
