ミトコンドリア膜中でのATP合成酵素と呼吸超複合体の超分子構造を高分解能で可視化
京都産業大学生命科学部横山謙教授ら研究グループは、ミトコンドリア内膜のATP合成酵素と呼吸鎖超分子複合体を生体膜を保ったまま高分解能で解析することに初めて成功しました。
■発表論文
「Structures of respiratory supercomplexes and ATP synthase oligomers in mammalian mitochondrial inner membrane」
(哺乳類ミトコンドリア内膜における呼吸鎖超複合体およびATP合成酵素オリゴマーの構造解明)
■概要
本研究では、ウシ心臓由来ミトコンドリアから調製したサブミトコンドリア粒子を用い、クライオ電子顕微鏡による単粒子解析によって、ミトコンドリア内膜タンパク質を、膜を壊さない本来の状態(ネイティブ状態)で構造解析しました。
その結果、ATP合成酵素(FoF1)がIF1タンパク質で連結された二量体として存在し、さらにそれらが会合した四量体構造がミトコンドリア内膜中に実在することを初めて明確に示しました。この四量体は膜を強く湾曲させ、ミトコンドリアのクリステ形成に重要な役割を果たすと考えられます。また、ATP合成酵素の回転リング中心に安定した脂質が存在するという従来の仮説は支持されませんでした。さらに、呼吸鎖超分子複合体について、従来知られていた構成に加え、CI1CIII2CIV₃という新規構成や、CI₂CIII₂CIV₆からなる巨大メガ複合体の存在を同定し、呼吸鎖複合体が多様な組み合わせで膜中に存在することを明らかにしました。
本成果は、ミトコンドリア膜タンパク質を少量試料からネイティブ状態で直接構造解析できる新たな手法の有効性を示すものであり、疾患関連ミトコンドリア研究や患者生検試料を用いた構造解析への応用、さらには膜タンパク質構造研究のパラダイム転換につながることが期待されます。
■背景
ミトコンドリアは、細胞内でATP(アデノシン三リン酸)を合成する「エネルギー工場」であり、生命活動に不可欠なアミノ酸、脂質といった物質の生産拠点でもあります。ミトコンドリア内膜には、ATP合成を担うATP合成酵素(FoF1)や、電子伝達を担う呼吸鎖複合体(複合体I~IV)が高密度に存在しています。これらの膜タンパク質は集合して超分子複合体を形成し、エネルギー産生の効率化に寄与すると考えられてきました。
しかし、これまでの多くの構造研究では、界面活性剤を用いて膜タンパク質を膜から取り出した試料が用いられており、生体膜中での実際の配置や集合状態(ネイティブ構造)は十分に解明されていませんでした。
■研究成果
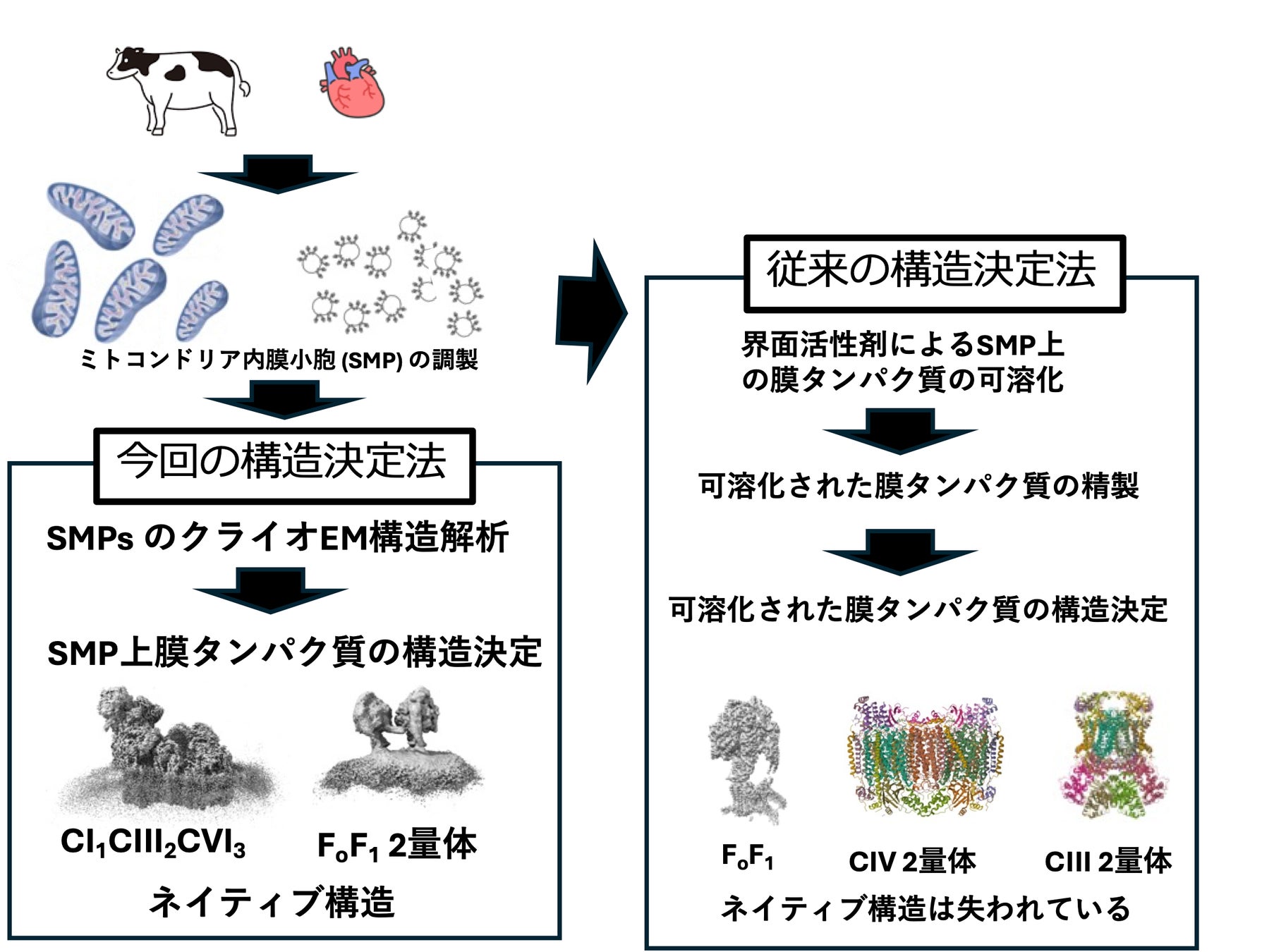
SMP上の膜タンパク質のネイティブ構造を決定(図1)
従来、膜タンパク質の構造決定は、生体膜を界面活性剤で可溶化し、得られた膜タンパク質をクロマトグラフィーなどで精製した後に行われてきました。この方法では、多量の試料と多大な労力を要するうえ、可溶化や精製の過程で、膜タンパク質の本来の会合状態や他因子との相互作用が失われる可能性がありました。
そこで本研究では、ウシ心臓由来ミトコンドリアから調製したサブミトコンドリア粒子(SMP)を用い、クライオ電子顕微鏡による単粒子解析を実施しました。膜構造を保持したまま解析することで、ミトコンドリア内膜タンパク質を、膜を壊さないネイティブ状態で構造解析することに成功しました。その結果、ATP合成酵素FoF1および呼吸鎖複合体のネイティブ構造を決定することができました。
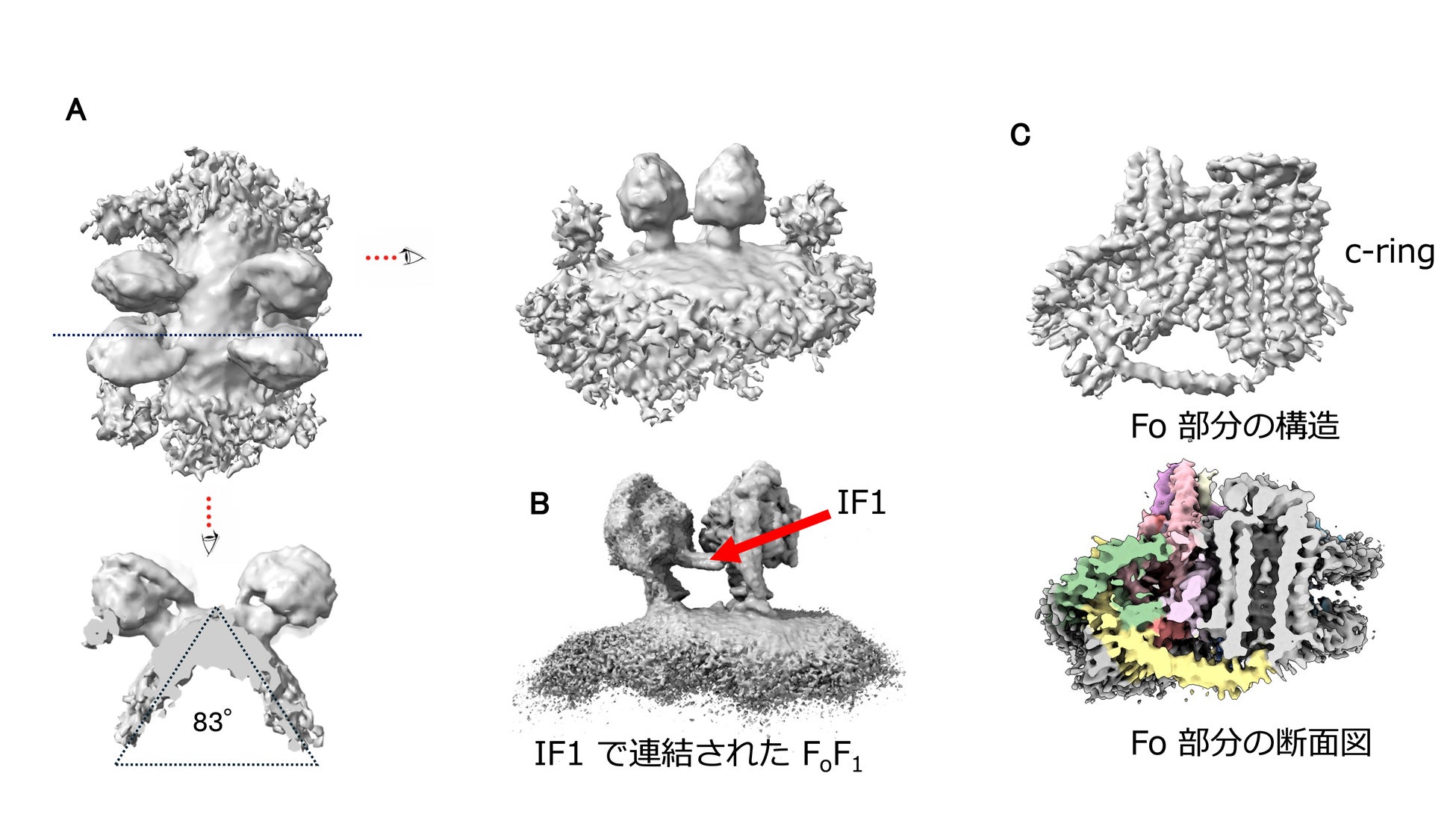
ATP合成酵素の高次構造の実在を証明(図2)
ATP合成酵素(FoF1)は、IF1と呼ばれる棒状タンパク質によって連結された二量体として存在することが確認されました。さらに、これらの二量体が会合した四量体構造が、ミトコンドリア内膜中に実際に存在することを明確に示しました。この四量体構造は膜を強く湾曲させる特徴を持ち、ミトコンドリア内膜に特有のひだ構造であるクリステ形成に重要な役割を果たしていると考えられます。従来、IF1で連結されたFoF1四量体は、精製過程で生じた人工構造の可能性が指摘されていましたが、本研究により生体内に実在する構造であることが実証されました。また、ATP合成酵素の膜内ローター部分(cリング)の中心に脂質が結合しているという仮説についても検証を行いましたが、安定した脂質の存在を支持する構造的証拠は得られませんでした。これまで脂質と考えられていた構造は、精製過程でリング内に入り込んだ界面活性剤である可能性が高いことが示されました。
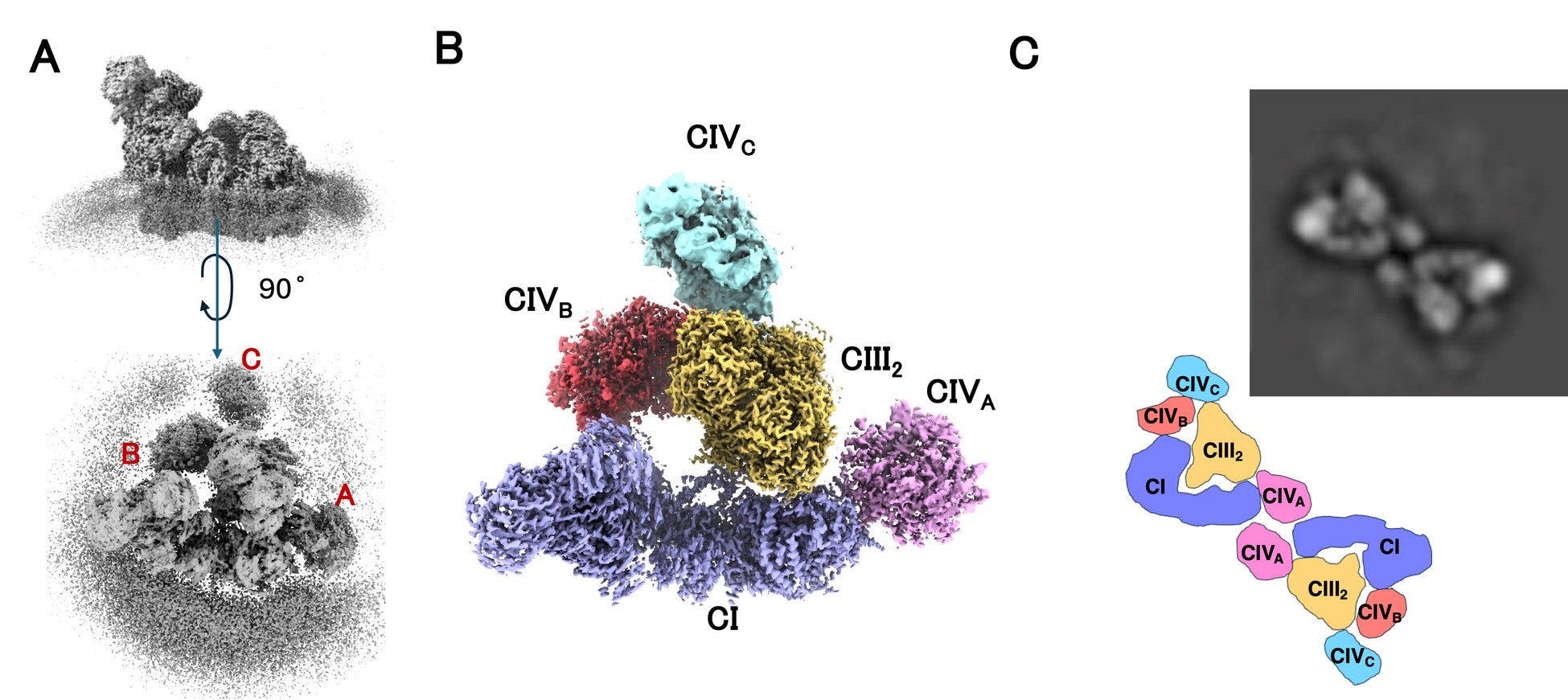
呼吸鎖超分子複合体の新規構成と多様性の発見(図3)
呼吸鎖複合体I・III・IVから構成される超分子複合体について、従来知られていた構成(CI₁CIII₂CIV₁、CI₁CIII₂CIV₂)に加え、CI₁CIII₂CIV₃という、これまで報告のなかった新たな構成を同定しました。さらに、2つの複合体Iを含む巨大なメガ複合体(CI₂CIII₂CIV₆)の存在も確認し、呼吸鎖複合体が固定的な構造ではなく、多様な組み合わせからなる超分子構造としてミトコンドリア内膜中に存在していることを明らかにしました。
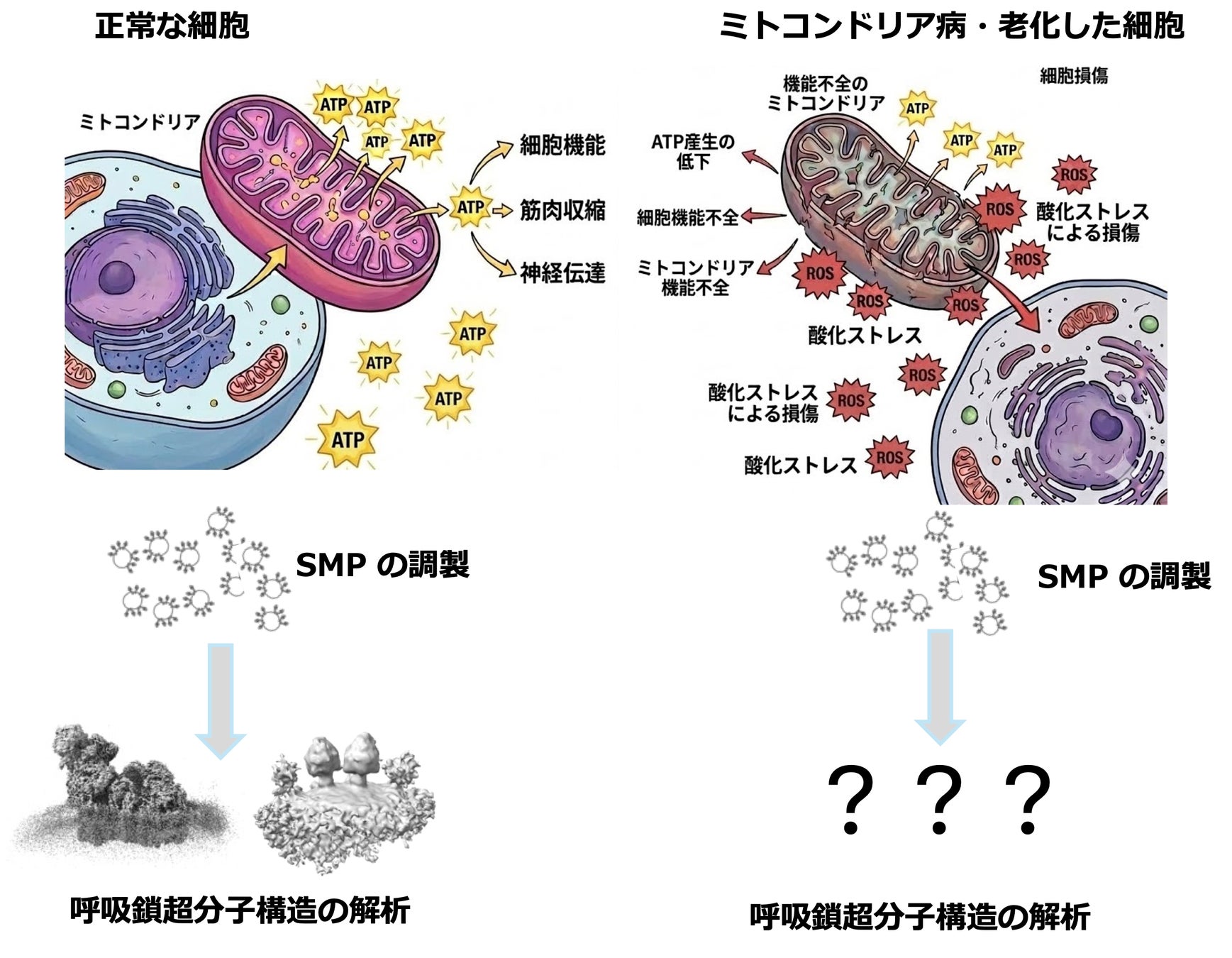
■研究の意義と今後の展望(図4)
本研究は、ミトコンドリア内膜タンパク質を「生体膜中に存在する本来の状態(ネイティブ状態)」で構造解析できるアプローチの有効性を示しました。この手法により、従来の精製法で得られた膜タンパク質の構造解析で見逃されてきた高次構造や集合様式を捉えることが可能になります。これまで、ミトコンドリア膜タンパク質の構造解析には大量のミトコンドリア試料が必要でしたが、本手法では少量のミトコンドリア膜からでもネイティブ構造を決定可能であることを示しました。これにより、大量調製が困難な実験動物組織や培養細胞などに由来するミトコンドリア膜タンパク質の構造解析への道が拓かれます。
ミトコンドリア機能異常は、ミトコンドリア病、糖尿病、神経変性疾患など多くの疾患と深く関わっています。本成果は、こうした疾患を構造生物学的視点から理解するための基盤となることが期待されます。
将来的には、患者由来試料を用いた解析や、アポトーシス(細胞死)過程におけるミトコンドリア構造変化の解明などへの応用が見込まれます。さらに、本研究はミトコンドリアに限らず、他の細胞内小器官に存在する膜タンパク質をネイティブ状態で解析できる可能性を示しており、膜タンパク質構造研究のパラダイム・チェンジをもたらす成果と位置づけられます。
■論文情報

|
論文タイトル |
Structures of respiratory supercomplexes and ATP synthase oligomers in mammalian mitochondrial inner membrane (哺乳類ミトコンドリア内膜における呼吸鎖超複合体およびATP合成酵素オリゴマーの構造解明) |
|
掲載誌 |
国際学術誌 Nature Communications |
|
掲載日時 |
2026年3月17日(火) |
|
著者 |
(1筆頭著者、2責任著者) 1中野 敦樹、1桝谷 貴洋、1秋定 晋輔、石川(福田)萌、光岡 薫、三芳 秀人、村井 正俊、2横山 謙 |
|
DOI |
■研究プロジェクトについて
本研究は、タンパク質動態研究所 (京都産業大学)、文部科学省科学研究費助成事業(23H02453 [横山]、25K01958 [村井])、武田科学振興財団 [横山]、住友ファーマ研究助成、マテリアル先端リサーチインフラ (ARIM) の支援を受けて行われました。
■用語・事項の解説
※1. クライオ電子顕微鏡法 (cryo electron microscopy)
急速凍結したタンパク質などの生体試料に電子線を照射し、試料の観察を行うために透過電子顕微鏡を行う。得られた2次元像から画像解析により、3次元再構成を行い、生体分子の立体構造を決定する。
※2. ATP (adenosine triphosphate)
様々な生体反応にエネルギー源として使われるため、細胞のエネルギー通貨とも呼ばれる。ヒトをはじめ多くの生物では、ATP合成のほとんどはATP合成酵素によって担われている。
※3. IF1タンパク質
IF1(Inhibitory Factor 1)は、ミトコンドリアATP合成酵素に結合する制御タンパク質で、ATP加水分解活性を抑制する役割を持つ。低酸素条件などでATP合成酵素が逆回転する際に結合し、細胞内ATPの無駄な消費を防ぐと考えられている。
※4. ミトコンドリアのクリステ構造
ミトコンドリア内膜は内側に折れ畳まれて「クリステ」と呼ばれるひだ構造を形成する。クリステは膜表面積を増大させ、ATP合成酵素や呼吸鎖複合体を高密度に配置することで、効率的なエネルギー産生を可能にしている。
※5. ATP合成酵素 (ATP synthase)
ATPの合成を担うタンパク質。真核生物の場合、ミトコンドリア内膜、細菌の場合は細胞膜に存在する。膜に埋まった部分で、生体膜内外に形成されたpH差を回転に変換し、膜から突き出た部分で回転力を使ってATPを合成する(図1)。回転によって反応を行うため、回転分子モーターとも呼ばれる。
※6. 呼吸鎖複合体 (respiratory complex)
呼吸鎖複合体とは、ミトコンドリア内膜に存在する複合体I~IVからなる膜タンパク質群で、電子伝達反応を通じてプロトン勾配を形成し、ATP合成を駆動する役割を担う。これらは超分子複合体として集合し、エネルギー産生効率の向上に寄与している。
※7. 膜タンパク質 (Membrane proteins)
その一部、または全体が生体膜の中に埋まっているタンパク質。細胞内外の情報伝達や物質の輸送などに関わる。タンパク質全体の約3割が膜タンパク質である。膜タンパク質は脂質二重膜中に存在するため、その構造解析には界面活性剤などで膜から可溶化する工程が必要とされてきた。しかし可溶化過程で、本来の配置や集合状態が失われることが多く、ネイティブ構造の解析は困難であった。
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像