「医薬品医療機器等法下で適応症を含む承認を取得した医療機器で調製された細胞加工物を用いる再生医療等技術の取扱いについて」における解釈に関して
令和4年10月5日付で厚生労働省より発出されました、「医薬品医療機器等法下で適応症を含む 承認を取得した医療機器で調製された細胞加工物を用いる再生医療等技術の取扱いについて」 (医政研発1005第1号厚生労働省医政局研究開発政策課長通知)につきまして、 学会員等から、解釈についての問い合わせがございましたので、注意喚起を含め、 ご連絡をさせていただきます。
当該通知には、以下の様に記載されております。
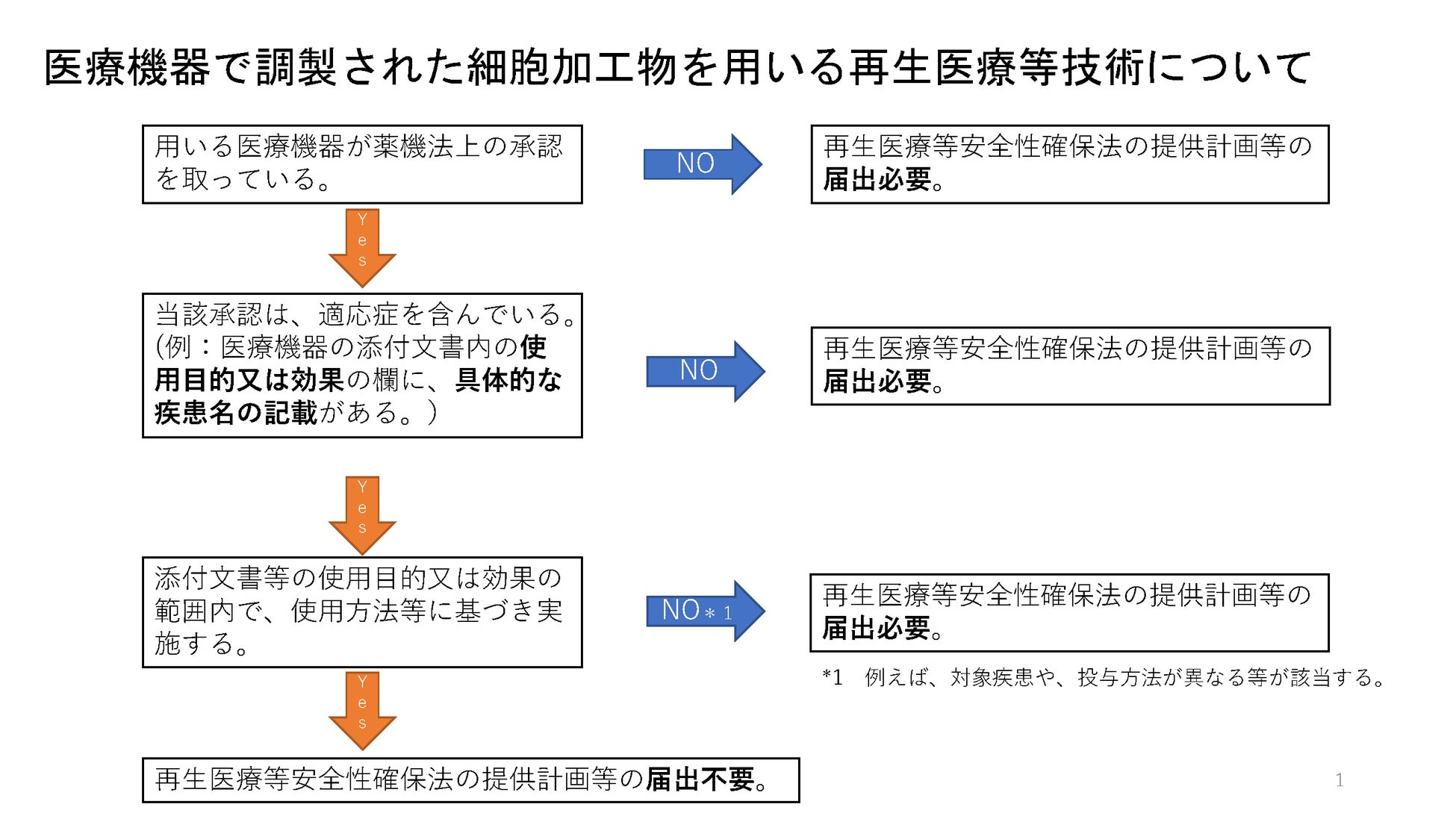
1 適応症を含む薬事承認を取得した医療機器のみをその薬事承認の内容に従い用いて再生医療等を提供する場合であって、その品質、有効性及び安全性を確保するために 求められる使用方法等について十分に留意しつつ提供が行われる場合には、薬機法による薬事承認及び再生法の規制の趣旨に鑑み、当該医療機器を用いる医療技術について再生医療等技術に該当しないものとして取り扱って差し支えないこと。
これは、細胞等を加工する医療機器において、今般、適応症を含む機器が薬事承認されたことを受けたものと考えられまして、当該医療機器を適応症に対する使用方法の範囲内で 用いる場合は、「再生医療等の安全性の確保等に関する法律」の対象とならず、 提供計画の届出等が不要となるという解釈ができるものと考えられます。ただし、
2 適応症を含む薬事承認を取得した医療機器をその薬事承認の範囲外で用いる場合及び 適応症を含まない薬事承認を取得した医療機器を用いる場合にあっては、引き続き、再生法による規制が適用されることに留意すること。
とあり、適応外の使用法を用いる場合は、引き続き法の対象となり、届出等も必要となる と考えられます。今後、細胞等を加工する医療機器を用いて再生医療を実施する方々に おかれましては、ご自身が購入、使用する医療機器の適応症、使用法を確認の上、届出等の 必要性の有無を適切にご判断いただくようにお願い申し上げます。
【医療機器で調整された細胞加工物を用いる再生医療等技術について】
https://bit.ly/3zRKY7b
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザーログイン既に登録済みの方はこちら
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
