厚生労働省が2025年も日本人の平均寿命発表!遺伝子でみる“生物学的年齢”、鍵になる栄養素とは?
エイジマネジメント研究に詳しい日比野佐和子医師に聞く
2025年7月25日、厚生労働省が発表した最新の「日本人の平均寿命」。数字の上では長生きできる時代になっていますが、私たちが本当に目指したいのは、「健康で若々しく歳を重ねること」ではないでしょうか。
そのために鍵を握るのが、日々の食事や適度な運動といった毎日の生活習慣ですが、最近では、遺伝子の働き方に影響を与える「エピジェネティクス(後天的な遺伝子制御の状態)」の視点から、生活習慣と健康や老化の兼ね合いを見つめ直す研究が進んでいます。
エピジェネティック(遺伝子的)な変化は、生活習慣や環境によって良くも悪くもなり得ます。たとえば若いうちは、食事や運動でその状態をリセットしやすいとされますが、長年にわたる不摂生やストレスが続くと、その影響が定着しやすくなり、簡単には元に戻らなくなることも。
イメージとしては、「遺伝子の上に貼られた付箋紙」。貼ったり剥がしたりして加えたり取り除いたりできる一方で、長く貼られていた付箋の跡が残るように、習慣の長期の積み重ねが解消できない健康障害につながることもあります。つまり、遺伝子への何らかの影響は「一度悪くなったら終わり」ではありませんが、早いうちに対策をとることで、より良い状態に戻せる可能性が、科学的にも示されつつあります。
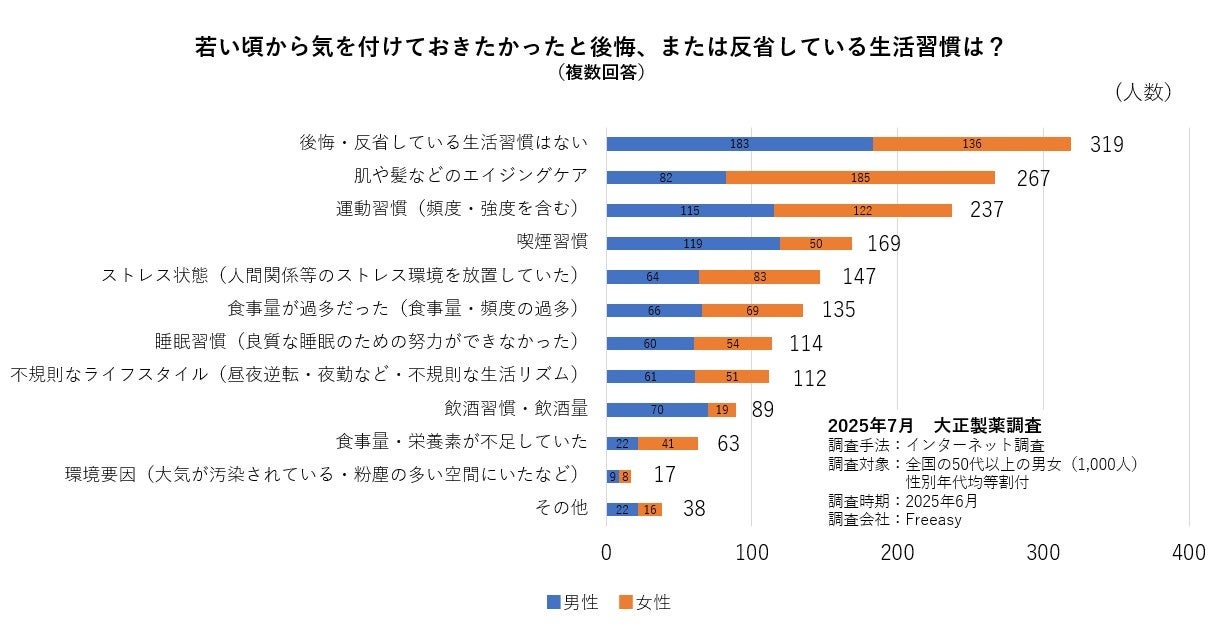
大正製薬が2025年6月に全国の50歳以上の男女1000人を対象に行ったアンケート調査によると、「若い頃から気を付けておきたかったと後悔、または反省している生活習慣は?」という質問に対して、3割以上の方が「後悔・反省している生活習慣はない」(319人)と回答していますが、後悔、または反省していることのトップ5は「肌や髪などのエイジングケア」(267人)、「運動習慣(頻度・強度を含む)」(237人)、「喫煙習慣」(169人)、「ストレス状態(人間関係等のストレス環境を放置していた)」(147人)、「食事量が過多だった(食事量・頻度の過多)」(135人)という順になりました。
生活習慣が健康にどう影響を及ぼすのか、「エピジェネティクス」の視点でとらえるとより具体的にその相関を解明できるようになるといいます。エイジマネジメント研究の専門家で、Rhelixa社の生物学的年齢検査「エピクロック®テスト」の科学顧問でもある日比野佐和子医師に、「エピジェネティクス」の視点で推奨できることを伺います。

【監修】 日比野佐和子先生
医療法人社団康梓会 SAWAKO CLINIC x YS 統括院長
大阪大学大学院医学系研究科未来医療学寄附講座 特任准教授
内科医、皮膚科医、眼科医、日本再生医療学会認定医、日本再生医療学会代議員、日本抗加齢医学会専門医。同志社大学アンチエイジングリサーチセンター講師、森ノ宮医療大学保健医療学部准教授、(財)ルイ・パストゥール医学研究センター基礎研究部アンチエイジング医科学研究室室長などを歴任。エイジマネジメント医療における第一人者として、最新の抗加齢医療、再生医療では専門的な知識と実績で、国内外のVIPの治療を担当。最先端の遺伝子検査を含む予防医療、ゲノム栄養学、分子栄養学指導などと、プラセンタ療法や幹細胞上清を用いたエクソソーム療法、各種美容皮膚科治療、美容内科治療、がん治療(免疫療法)、ホルモン補充療法、点滴療法など多岐にわたる診療を行う。プラセンタ療法を含む再生医療においてのパイオニアでもある。
エピゲノム解析で今後さらに明らかになる、食と生活習慣の重要性
近年、生活習慣が遺伝子の発現にどのような影響を与えるかを調べる技術も進化しています。私は生物学的年齢と食事・運動・睡眠・ストレスなどの生活習慣がDNAにどんな影響を与えるかを解析できる先進的なRhelixa社の生物学的年齢検査「エピクロック®テスト」の科学顧問として、食事・運動・睡眠・ストレスなどの生活習慣と生物学的年齢、将来の予測寿命との関連を解析するプロジェクトに関わっています。
私たちの遺伝子は、本来もっている「健康を維持するための正しい働き方」を備えています。ところが、長年にわたる不摂生な食生活やストレス、睡眠不足、喫煙などの悪い生活習慣が続くと、その影響が「エピジェネティックな変化」として蓄積され、遺伝子の働きが本来のバランスから乱れてしまいます。
これは、いわば“遺伝子のスイッチ”が誤ってオン・オフされるような状態です。たとえば、本来ならば活発に働いてほしい細胞修復や抗炎症の機能をもつ遺伝子が沈黙してしまったり、逆に炎症を引き起こす遺伝子が過度に活性化したりすると、病気や老化のリスクが高まります。
近年の研究では、特定の栄養素や生活習慣の改善を通じてこのような「エピジェネティクス」を“書き換える”こと、「エピジェネティック・リプログラミング」が可能であることが分かってきました。今後、さまざまな栄養素に関して、「エピジェネティック・リプログラミング」への寄与が解明されていくと考えます。これまでの解析から、「魚介類中心の食生活」、「定期的な有酸素運動」、「良質な睡眠環境」が、より若々しいエピジェネティック年齢と相関していることが示されています。
つまり、食事や生活環境を意識的に整えることが、遺伝子レベルでの老化防止や健康維持につながることが、今後遺伝子レベルで明らかになるのです。私たちの毎日の選択が、見た目や体の調子だけでなく、遺伝子レベルにまで影響を与えているという事実を、プロジェクトを通して強く実感しています。
長寿につながることが期待される食事とは
遺伝子のはたらきを正しく制御してくれる栄養素が判明すれば、食生活によって「老化のスピードを緩やかにし、より健康的な体の状態に近づける」ことが不可能でないといえます。
長寿を目指すなら、まずはバランスの良い食事が土台です。なかでも、地中海沿岸地域の伝統的な食生活「地中海食」は、世界中の研究者がアンチエイジング対策として推奨していますが、この食習慣の有効性も、エピジェネティクス研究によってあらためて証明されていくと思います。
地中海食は、魚介類、オリーブオイル、ナッツ類、野菜、果物、全粒穀物、豆類などを中心に構成され、赤身肉や加工食品は控えめ。こうした食事スタイルは、良質な脂質や食物繊維、そして多様なポリフェノールを豊富に含んでおり、細胞レベルでの炎症や酸化ストレスを抑える効果が期待されています。実際にスペインで行われた大規模な臨床研究(※1)でも、魚介類を頻繁に摂り、赤肉・加工肉は週1回未満に抑え、毎日30gのナッツ、大さじ4杯のオリーブオイル、全粒穀物を主食にすることで心血管疾患の予防効果が得られると実証されました(※2)。
魚、イカ、タコ、ホタテなど魚介類に豊富に含まれる「タウリン」は、細胞の浸透圧を整え、自律神経を安定させるとともに、強力な抗酸化作用も発揮します。中年マウスの実験では、骨密度の低下の抑制(※3)や筋力や代謝、認知機能にも改善が見られ、健康寿命が延びる明確な証拠となりました。テロメアを伸長させる酵素(テロメラーゼ)の欠損に伴う老化に対してタウリンが抑制的に働くということも示唆されており(※4)、世界的にもエピジェネティックに関与する可能性が期待されています。
さらに、美容医療などでも注目される「L-システイン」や「グルタチオン」は、体内の抗酸化環境を高め、ターンオーバー(細胞の生まれ変わり)を整える働きがあります。これらは肌の再生を促し、老廃物の排出(デトックス)を助けることで、内側からの美しさにもつながります。サプリメントや点滴などで取り入れられるほか、レバー、ブロッコリー、アボカドといった食品にも多く含まれています。
オリーブオイルには抗酸化作用の高い「ポリフェノール」と「オレイン酸」が含まれ、細胞の老化を防ぎます。ナッツ類(特にくるみやアーモンド)は、ビタミンEやマグネシウムなどを豊富に含み、抗酸化・抗炎症作用に期待できます。
野菜や果物には、ビタミンCやカロテノイド、葉酸が含まれ、細胞の修復や免疫強化に貢献します。特に果物に多いポリフェノールは、エピジェネティックな遺伝子発現のコントロールにも関与していると考えられています。(※5)
全粒穀物は、ビタミンB群や食物繊維が豊富で、代謝や腸内環境を整えることで遺伝子のスイッチの正常化を助けます。
また、豆類は植物性たんぱく質や鉄分、イソフラボンなどを含み、ホルモンバランスや抗炎症作用に寄与します。
加えて、サケやサバなどの脂の乗った魚や、きのこ類(干ししいたけなど)、卵黄に多く含まれるビタミンDは免疫調整作用があり、エピジェネティックな変化にも関与することが示唆されています(※6)。青魚(サバ、イワシ、サンマなど)やアマニ油、えごま油、チアシードなどが代表的な摂取源であるオメガ-3脂肪酸は、抗酸化作用を発揮します。(※7)です。牡蠣や、大豆製品、カシューナッツに豊富な亜鉛も、傷ついたDNAの修復や免疫調整に不可欠なミネラルといわれます。(※8)
ヨーグルト、キムチ、納豆といった発酵食品も、遺伝子の働きを支えるうえで役立ちます。乳酸菌やビフィズス菌によって腸内フローラのバランスを整えることで、免疫細胞の7割が集まると言われる腸内環境が整い、免疫力や代謝を安定させます。これらは間接的にエピジェネティックな調整にも関与するといえるのではないでしょうか。
これらの食品を日常的に取り入れることで、生物学的年齢を若々しく保つ土台が整うと考えています。
将来的には、個人のエピクロック検査結果に合わせて、必要な食事を個別に提案したり、サプリメントや食事療法で遺伝子の働き方を調整したりするパーソナライズド栄養指導や予防医療への応用が期待されています。栄養素の効果を個人の「エピジェネティクス」の組み合わせにより、より精緻な長寿戦略を提案できる時代が訪れるでしょう。
エピゲノムへのポジティブな影響が期待される “3つの生活習慣”
エピジェネティクスの観点では、食生活のみならず、毎日の行動が遺伝子に与える影響が注目されています。特定の生活習慣は、遺伝子スイッチの“良い方向”への制御に寄与し、生物学的年齢の若返りや病気予防につながると考えられています。ここでは、エピゲノムを改善させることを目指す3つの基本習慣について目安を紹介します。
1.運動
毎日1万歩程度のウォーキングなどの適度な運動は、テロメア(染色体の末端にある遺伝情報を保護する「キャップ」のような役割を持ち、細胞が分裂するたびにこのテロメアは少しずつ短くなり、一定以上短くなると細胞の分裂が止まり、老化や機能低下につながる)の短縮を抑制し、生物学的年齢を若返らせる効果が期待されるといわれています。(※9)
2.睡眠
室温は外気との温度差を5℃以内(例:外気35℃なら室温28〜29℃)に設定し、41℃以下の湯船にゆっくり浸かることで副交感神経を優位にして、質の高い深い睡眠を確保しましょう。
3.環境(ストレス管理)
化学物質を極力排した住環境の整備や、週1回、自分の趣味を取り入れて、楽しいことをしたり、スケジュールを詰めすぎずに自由に過ごすなどのリラックスタイムで気持ちを切り替えることも、ストレスの軽減につながり、エピジェネティックに良い影響を与えることにつながると考えられます。
「エピジェネティック」視点で、今からでも食習慣・ライフスタイルを見直しましょう
長寿において遺伝要因の寄与率は25~30%とされ、残りの70~75%は生活習慣などの環境因子にあるともいわれます。(※10)手遅れになる前に、少しでも早く、食習慣や生活習慣を改善することが、未来の自分をより若々しく保つ第一歩になります。
●Rhelixa社 生物学的年齢検査「エピクロック®テスト」 https://epiclock.jp/
※1 PREDIMED試験(Estruch, R. et al. 2013)『Primary prevention of cardiovascular disease with a Mediterranean diet』NEJM, 368(14), 1279–1290。
※2 全粒穀物介入研究(García-García I. et al. 2024)『Examining nutrition strategies to influence DNA methylation and epigenetic clocks: a systematic review of clinical trials』Frontiers in Aging, 5:1417625。
※3 タウリン老化マウス試験(Yadav, M. et al. 2023)『Taurine deficiency as a driver of aging』Science, 380(6649), eabn9257.
※4 タウリンは、テロメラーゼ欠損による老化促進や死亡率上昇を抑制することが、ゼブラフィッシュなどのモデル動物で確認されている。タウリン補給により、テロメア短縮に伴う細胞老化や個体死を軽減し、老化関連マーカーを改善する効果が示された。(Singh, P. et al. 2023. Taurine deficiency as a driver of aging. Science, 380(6650), eabn9257. https://doi.org/10.1126/science.abn9257)
※5 ポリフェノールの摂取がエピジェネティックな加齢に与える影響 GreenMED試験(Berson, A. et al. 2023)『The effect of polyphenols on DNA methylation-assessed biological age』BMC Medicine, 21(1), 240。
※6 ビタミンDとエピジェネティクス研究(Carlberg C. et al. 2012)『Vitamin D and the epigenome』Frontiers in Physiology, 3:164。
※7 オメガ-3脂肪酸補充試験(Clarke-Harris R. et al. 2017)『Long-chain polyunsaturated fatty acids and DNA methylation in adult humans: a systematic review of randomized controlled trials』Clinical Epigenetics, 9:43。
※8 亜鉛とDNA修復研究(Song Y. et al. 2009)『Zinc and the DNA damage response in human health and disease』Mutation Research, 733(1–2), 111–121。
※9 運動とテロメアの関係研究(Puterman E. et al. 2010)『The power of exercise: buffering the effect of chronic stress on telomere length』PLoS ONE, 5(5), e10837。
※10 寿命における遺伝的影響の推定は多くの双子研究や家系分析に基づき、全体の寿命差のうち15〜30%が遺伝で説明されるとされる。(Herskind, A. M. et al. 1996. The heritability of human longevity: A population-based study of 2872 Danish twin pairs born 1870–1900. Human Genetics, 97, 319–323)。
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像