角膜上皮障害の修復メカニズムを解明
~非ステロイド性消炎鎮痛剤点眼薬の副作用治療への道筋~
- 非ステロイド性消炎鎮痛剤は12-HHT産生を抑制することで角膜上皮損傷の修復を遅延させる
- BLT2作動薬は角膜上皮細胞の移動を促進することで角膜上皮障害の修復を促進する
- 難治性角膜上皮障害の新規治療法につながる研究成果
【背景】
眼球の前面に存在する角膜は常に外界に接しており、微生物や異物の侵入から眼全体を保護するバリアとして機能していますが、コンタクトレンズの使用や異物の侵入、外傷などによって角膜上皮障害が生じることがあります。また、非ステロイド性消炎鎮痛剤(NSAIDs)を含む点眼薬は白内障手術の術後などに頻用されていますが、その副作用として角膜上皮びらんや重症例では角膜穿孔を生ずることが問題となっています。
研究グループは、これまで生理活性脂質とその受容体の研究を行ってきました。その過程で、2000年に腸管上皮細胞や皮膚ケラチノサイトに発現する新規のGタンパク質共役型受容体(*4)を発見し、BLT2と命名しました。BLT2を活性化する生体内リガンドの探索を行った結果、2008年に12-HHTと呼ばれる脂肪酸を同定しました。その後、BLT2が皮膚ケラチノサイトに発現し皮膚の創傷治癒を促進するとともに、皮膚のバリア機能維持に必須であることを明らかにしました。
研究グループでは、BLT2の皮膚の創傷治癒の促進作用に着目し、眼の角膜上皮障害にも有用ではないかと考えました。そこで本研究では、NSAIDs点眼薬の副作用の角膜上皮障害の実態と、その修復における12-HHT/BLT2の役割を明らかにする研究を行いました。
【内容】
まず、マウスの角膜におけるBLT2の発現を調べたところ、BLT2が皮膚に匹敵する高いレベルで角膜組織に発現していること、そのリガンドである12-HHTが豊富に眼に存在していることを確認しました。角膜上皮障害への12-HHT/BLT2の役割を明らかにするため、角膜上皮を直径2mmにわたって剥離し、経時的に損傷上皮の面積を計測するという角膜損傷修復モデルを作製しました。NSAIDsであるジクロフェナクを含む点眼薬を投与すると角膜上皮損傷の修復が遅延し(図1A)、一方、BLT2を活性化する12-HHTや合成BLT2作動薬の点眼によって修復が促進する(図1B)ことを発見しました。なお、BLT2欠損マウスの角膜上皮損傷修復は、野生型マウスと比較して大きく遅延しており、ジクロフェナク点眼による更なる遅延は観察されませんでした。さらに、ヒト初代培養角膜細胞やBLT2を発現させた角膜細胞を用いた試験管内創傷治癒モデルでも12-HHTによる創傷治癒の促進効果が観察されました。
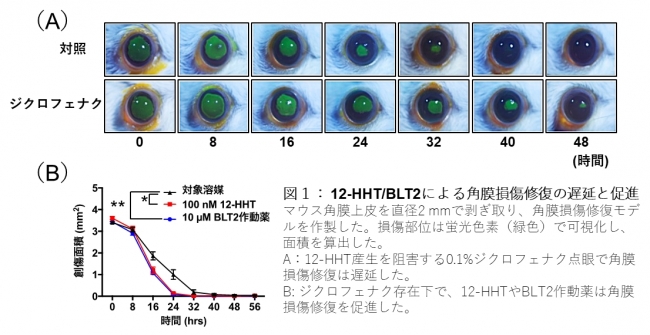 図1:12-HHTBLT2による角膜損傷修復の遅延と促進
図1:12-HHTBLT2による角膜損傷修復の遅延と促進
以上の結果から、1)NSAIDsによる角膜上皮損傷修復の遅延は、プロスタグランジンの産生阻害ではなく、12-HHTの産生阻害という新しいメカニズムで生じていること、2)BLT2作動薬が角膜上皮損傷の新規治療薬となる可能性があることが明らかとなりました。
【今後の展開】
NSAIDsの副作用で角膜障害や角膜上皮損傷修復の遅延が生じるメカニズムはこれまで明らかではなく、本研究による12-HHT産生阻害のメカニズム(図2)が世界で初めての報告となります。角膜外傷やコンタクトレンズ使用者、糖尿病で生じる角膜潰瘍に対する治療薬についてはアンメットニーズがありますが、本研究グループが発見した合成BLT2作動薬が、角膜潰瘍の新規治療薬として臨床応用されることが期待されます。
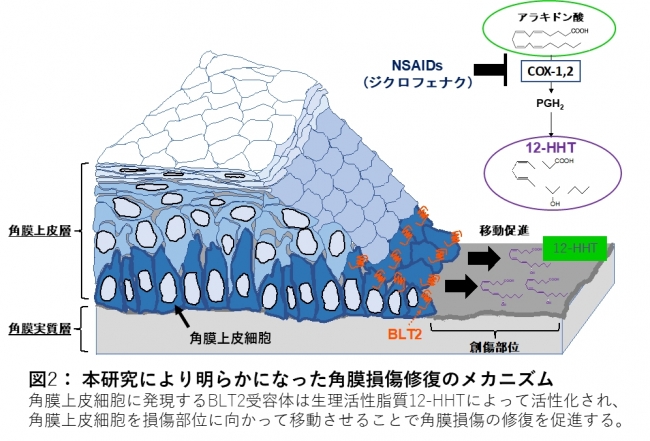 図2:本研究により明らかになった角膜損傷修復のメカニズム
図2:本研究により明らかになった角膜損傷修復のメカニズム
【用語解説】
*1 生理活性脂質12-HHT
12-ヒドロキシペプタデカトリエン酸の略。血液凝固時に主として血小板から大量に産生される炭素数17の不飽和脂肪酸。細胞膜に存在するアラキドン酸という脂肪酸から細胞内の酵素反応によって産生される。横溝教授らの研究によって、生物学的な活性がはじめて報告された。
*2 BLT2
この受容体は、2000年の発見の際、別の生理活性脂質であるロイコトリエンB4(LTB4)に対する低親和性受容体であることが分かり、高親和性受容体であるBLT1と区別するため、BLT2と命名された。その後2008年に、より親和性の高い生体内リガンドとして12-HHTが発見された。
*3 NSAIDs
非ステロイド性消炎鎮痛剤(NonSteroidal Anti Inflammatory Drugs)の略称。アスピリン、イブプロフェン、ロキソプロフェンなど、シクロオキシゲナーゼを阻害しプロスタグランジン産生を抑制することで、解熱鎮痛作用を発揮する。短時間で効果を発揮するが、消化管粘膜障害、血液凝固阻害、陣痛発来遅延などの副作用が知られている。
*4 Gタンパク質共役型受容体
GPCRとも称され、ヒトゲノムには約1,000種類のGPCRがコードされている。それぞれが特異的なリガンドによって活性化されると考えられているが、リガンドが同定されているものは約300程度である。重要な創薬標的とされており、現在、臨床医学の現場で使用されている薬剤の約半数は、何らかのGPCRを標的とした薬剤である。
【原著論文】
本研究は、Nature Publishing Groupの電子版雑誌「Scientific Reports」(www.nature.com/articles/s41598-017-13122-8)で日本時間:2017年10月16日18時に公開されました。
英文タイトル: Non-steroidal anti-inflammatory drug delays corneal wound healing by reducing production of 12-hydroxyheptadecatrienoic acid, a ligand for leukotriene B4 receptor 2
日本語訳: 非ステロイド性消炎鎮痛剤は、ロイコトリエンB4第二受容体リガンドである12-ヒドロキシエイコサテトラエン酸の産生抑制を介して、角膜創傷治癒を遅延させる。
著者: Satoshi Iwamoto, Tomoaki Koga, Mai Ohba, Toshiaki Okuno, Masato Koike, Akira Murakami, Akira Matsuda, Takehiko YokomizoSci. Rep. (2017) doi: 10.1038/s41598-017-13122-8
なお本研究は、文部科学省JSPS科研費(新学術領域研究JP22116001、JP22116002、JP15H05901、JP15H05904、基盤研究B JP15H04708)、私立大学戦略的研究基盤形成支援事業、武田科学振興財団の支援を受け実施されました。
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
- 種類
- その他
- ダウンロード
