CRO事業の拡大に向けたArkMS株式会社による株式会社エムウィズとの業務提携について
当社の子会社であるArkMS株式会社(アークメディカルソリューションズ、本社:東京都豊島区、代表取締役社長:水尾斉、以下「ArkMS」)は、株式会社エムウィズ(本社:大阪府大阪市、代表取締役社長:杉本俊一、以下「エムウィズ」)と、医薬品および医療機器の安全性関連サポート業務とその営業活動に関する業務提携基本契約を締結しましたので、下記のとおりお知らせいたします。
記
1.背景と目的
2024年7月に厚生労働省から発出された通知※1では、承認審査の過程や製造販売後に、評価すべき具体的な検討事項が生じていない場合は、製造販売後の有効性については製造販売後調査等によらない、文献の分析等による方法で評価しても差し支えないとされています。一方、治験症例数が限られている場合は、PMS※2の重要性が高く、継続的な安全性評価や適正使用の推進が重要となります。加えて、市販後の安全性関連サポート業務の高度化に伴い、定型的な市販後調査を超えたプランニングやコンサルティング、そしてRMP※3関連資材の作成やメディカルライティング※4へのニーズが高まっています。
アルフレッサグループは、医薬品等の導入・開発、製造から物流・販売、市販後調査(PMS)・ラストワンマイルまでをグループ一体となって提供するトータルサプライチェーンサービス(以下「TSCS※5」)を事業戦略の柱に位置付け、海外の新興バイオ医薬品企業等による日本市場への参入を包括的に支援するプラットフォーム「PATH-Solution(商標出願中)」のサービスを提供しております※6。TSCSにおいて、CRO※7としての機能を担うArkMSは、医薬品等の開発支援を行い、医薬品・医療機器・再生医療等の分野で、臨床試験・医師主導治験から製造販売後調査に至るまで、包括的に高品質なソリューションを展開しています。
このたびの業務提携により、製薬企業での実務経験を有する両社の専門人財を結集させ、エムウィズが強みとするGVP※8とGPSP※9領域におけるPMS、PV※10およびメディカルライティング等における両社の体制をより一層強化し、品質や提案力の向上を目指します。また、営業ネットワークを共有することで、既存のお客様への提案機会に加え、新規の商談機会の拡大につなげます。これらを通じて、ArkMSのCRO事業とTSCSの機能のさらなる拡充を進めてまいります。
※1 ご参考:厚生労働省「医薬品の製造販売後調査等の実施計画の策定に関する検討の進め方について」
https://www.mhlw.go.jp/content/11120000/001318112.pdf
※2 PMS:(Post Marketing Surveillance)医薬品や医療機器が販売された後に行われる品質、有効性および安全性の確
保を図るための調査
※3 RMP:(Risk Management Plan)医薬品リスク管理計画書
※4 メディカルライティング:治験総括報告書や医薬品の承認申請資料、学会発表資料など、医学・薬学的な専門文書を科
学的妥当性と整合性を担保して作成する業務
※5 TSCS:アルフレッサグループ全体で保有する様々な機能を有機的に一体活用することで、シームレスなサプライチェー
ンを確立し、医薬品等の導入・開発、製造から、物流・販売、市販後調査・ラストワンマイルまでをグループ一体とな
って提供することを指しています。
※6 ご参考:2026年1月30日発表
「ドラッグ・ラグ/ロス」の解消へ向けた 海外新興バイオ医薬品企業等の日本参入支援プラットフォーム
「PATH-Solution」 サービス提供開始のお知らせ
https://ssl4.eir-parts.net/doc/2784/ir_material15/272407/00.pdf
※7 CRO:(Contract Research Organization)製薬企業や研究機関が行う臨床試験に関する一連の業務を支援する専門
機関
※8 GVP:(Good Vigilance Practice)市販後の医薬品・医療機器等の安全管理情報を収集・検討し、安全確保措置を実施
するための省令
※9 GPSP:(Good Post-marketing Study Practice)市販後の医薬品安全性を確認するため、使用成績調査やデータベー
ス調査等の実施方法・手順を定めた日本独自の省令
※10 PV:(Pharmacovigilance):医薬品安全性情報管理
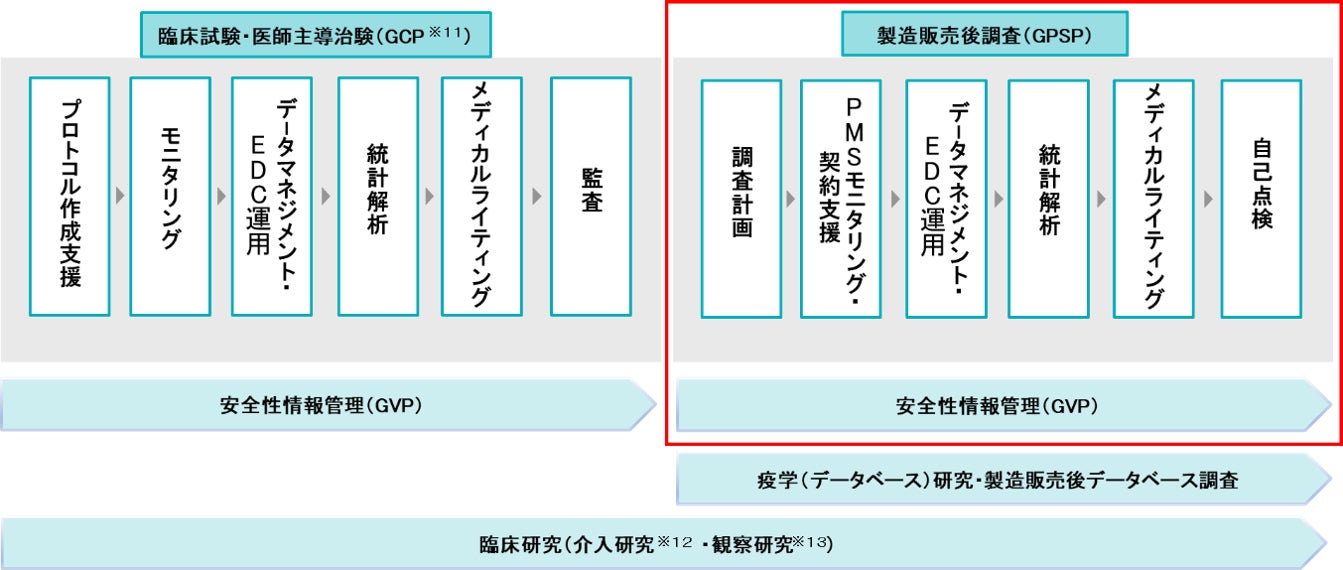
【本件で強化されるArkMSの機能】
(注)赤枠が主に強化される領域
※11 GCP:(Good Clinical Practice)医薬品の臨床試験を倫理的かつ科学的に実施し、データの信頼性を確保するため
の国際的な基準・規制
※12 介入研究:疾病と因果関係があると考えられる要因について、対象者に対して研究者が新しい治療などの介入を行い、
従来の治療などと比較してその有効性を検証する研究のこと
※13 観察研究:研究者が介入をせず、対象者の健康・疾病に関するデータを収集・分析して新しい知見を得る研究のこと
2.業務提携の内容
本提携により、ArkMSとエムウィズが共同で、主に医薬品および医療機器の安全性関連サポート業務における以下のサービスを提供します。
(1)メディカルライティング業務
(2)PMSに関するプランニング支援業務
(3)PVおよびPMSに関わるコンサルティング業務
(4)RMPまたは適正使用情報提供に関わる資材等の製作
(5)データマネジメントおよび統計・解析業務
(6)その他、両社が合意した業務
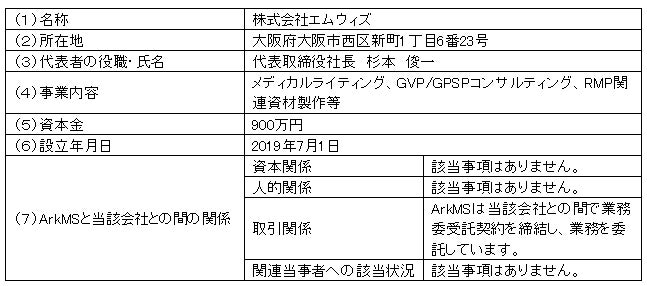
3.相手先(エムウィズ)の概要(2025年1月31日現在)
4.業務提携契約締結日
2026年3月31日
5.今後の見通し
本件による今期業績へ与える影響は、軽微であると見込んでおりますが、中長期的には当社グループの企業価値向上に資するものと考えております。
今後、本件に関して開示すべき事項が生じた場合には速やかにお知らせいたします。
以 上
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
