愛知県がんセンター、聖マリアンナ医科大学病院、MICIN、がん領域で注射治験薬における本邦初 完全リモートのオンライン治験を実装
愛知県がんセンター(所在地:愛知県名古屋市、病院長:山本 一仁)、聖マリアンナ医科大学病院(所在地:神奈川県川崎市、病院長:大坪 毅人)、株式会社MICIN(本社:東京都港区、代表取締役:原聖吾、以下「MICIN」)は、本邦初となる、がん領域で注射治験薬における完全リモートのオンライン治験(DCT: Decentralized Clinical Trials)の実施を開始します。本実装では、かかりつけ病院(パートナー医療機関)と連携した上で、MICINのDCTプラットフォーム「MiROHA(ミロハ)システム」を活用し、患者さんは治験実施医療機関の愛知県がんセンターと聖マリアンナ医科大学病院に一度も来院することなく治験に参加することができます。本取り組みを通じて患者さんの治験参加アクセスを大幅に向上させることを目指します。

【背景】
都市部の医療機関に治験が集中する一方で、地方の患者さんは治験に参加するために長距離移動を強いられることが多く、通院負担の大きさが治験参加の障壁となっています。その結果、日本の治験は症例登録の遅延や治験期間の長期化といった課題を抱え、ドラッグラグやドラッグロスの一因となっています。また、がん領域では、全国のがんゲノム医療中核拠点病院・拠点病院・連携病院で「がん遺伝子パネル検査」を保険診療で受けることができます。しかし、治療標的が見つかっても、近隣に治験実施施設がないため治験参加を断念せざるを得ない患者さんがいることが、大きな課題となっています。
この課題の解決に向けて、愛知県がんセンターでは、本邦初の試みとして、内服薬を用いた医師主導治験における完全リモートのオンライン治験を実現しました (1)。さらに、企業主導治験において、愛知県がんセンターならびに聖マリアンナ医科大学病院とMICINは、医療機関のネットワークと「MiROHA」を活用した遠隔プレスクリーニングの取り組みを実装しました(2)(3) 。
これまで、内服薬を用いた治験では、一度も通院せずに参加できる完全オンライン治験が可能でした。しかし、注射薬の治験では遠隔プレスクリーニングは可能なものの、治験薬の投薬には治験実施医療機関への来院が必要であることが課題でした。今回、これまでの知見を活かし、愛知県がんセンター、聖マリアンナ医科大学病院、MICINは、本邦初となるがん領域における注射治験薬の完全オンライン治験を実施する運びとなりました。
【本取り組み】
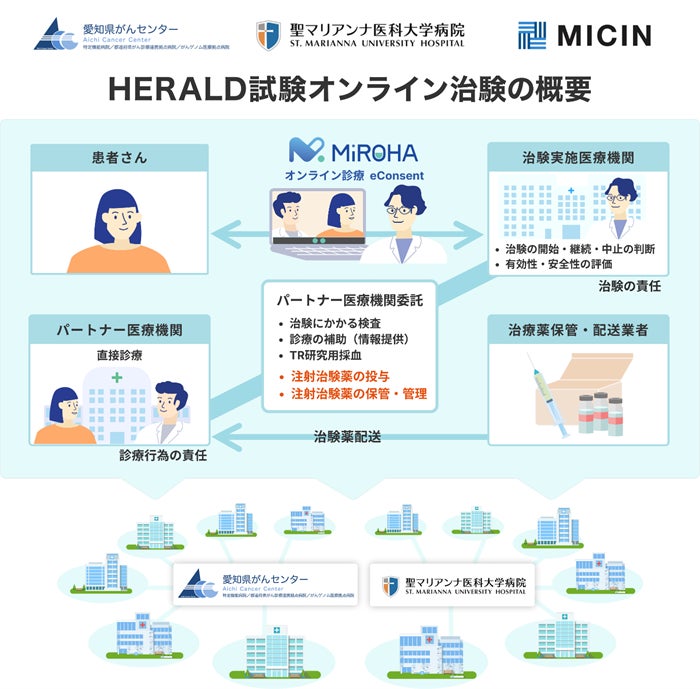
がん遺伝子パネル検査でHER2遺伝子増幅が認められる固形がん患者さんを対象に、トラスツズマブデルクステカン(注射治験薬)の有効性と安全性を調べる医師主導治験(HERALD試験)(4) にオンライン治験を導入します。治験実施医療機関への通院が難しい患者さんに対し、かかりつけ病院(パートナー医療機関)と連携し、「MiROHA」を活用したオンライン診療および遠隔での説明・同意取得を実施します。治験で定められた血液検査、画像検査、治験薬の投与は、治験実施医療機関(愛知県がんセンター、聖マリアンナ医科大学病院)の指示のもと、かかりつけ病院で行います。治験実施医療機関の担当医師、治験コーディネーター、薬剤師は、かかりつけ病院の医療者と協力し、安全な治療の提供に努めます。
【今後の展望】
本取り組みにより、日本全国の患者さんが遠方にお住まいでも治験に参加することが可能になります。まずは医師主導治験で注射治験薬におけるフルリモート型オンライン治験を実装開始し、本邦初の先駆的な実装で得られる知見を活かし今後企業治験にも展開することで、国内の臨床試験環境全体の発展に繋げていくことを目指します。
愛知県がんセンター、聖マリアンナ医科大学病院、MICINは、今後もIT技術を活用したオンライン治験の実施を進め、より多くのがん患者さんが最新の治療にアクセスできる環境・体制整備に向けた取り組みを加速し、日本の治験環境の国際競争力を高めてまいります。
【出典】
(1) かかりつけ病院と協力して患者さんとオンライン診療を行う完全リモート治験を開始します https://cancer-c.pref.aichi.jp/wp/wp-content/uploads/r40214-1.pdf
(2) 愛知県がんセンター、武田薬品、東北大学病院、MICIN 治験におけるeConsentを用いたプレスクリーニングの開始について https://cancer-c.pref.aichi.jp/wp/wp-content/uploads/20241009.pdf
(3) 聖マリアンナ医科大学病院・アムジェン・MICIN、がんの企業治験でMICINの「MiROHA(ミロハ)eConsent」を使用開始 がん領域における分散型臨床試験(DCT)の実現を目的として https://www.marianna-u.ac.jp/houjin/today/20240201_01/01.pdf
(4) リキッドバイオプシーによりHER2遺伝子増幅が認められた固形がんに対するトラスツズマブデルクステカンの臓器横断的な有効性を確認―産学連携SCRUM-Japan MONSTARプロジェクトの成果を米国臨床腫瘍学会旗艦誌「Journal of Clinical Oncology」に論文発表―
https://cancer-c.pref.aichi.jp/news_press-release/12943/
【各施設・企業】
愛知県がんセンターに関して
愛知県がんセンターは1964年にがん研究会、国立がん研究センターに次いで設立され、我が国の3大comprehensive cancer center(病院と研究所を併設する総合がんセンター)の一つとして、60年余に渡って実績と信頼を築いて来ました。病院と研究所が併設されている強みを存分に活かし、科学的なエビデンスをもとに、現在ある最良の医療を提供するとともに、新しいエビデンスの創出、明日のより良い医療、がんにならないための予防法の創出に向け、まい進しています。詳細については、https://cancer-c.pref.aichi.jp/ をご覧ください。
聖マリアンナ医科大学病院に関して
「生命の尊厳を重んじ、病める人を癒す、愛ある医療を提供すること。」を理念に掲げ、特定機能病院としての役割を果たすべく、高度な医療安全管理体制のもと、高難度手術や高度医療の提供およびその開発・研修を行っています。2023年1月からは新たな入院棟がオープンし、診療体制が拡充されました。2025年1月の外来棟リニューアルオープン、2027年春のグランドオープンと続き、患者さん・時代・社会から必要とされる地域中核病院として、より一層の発展を目指します。
ホームページ:https://www.marianna-u.ac.jp/hospital/
MICINに関して
MICINは「すべての人が、納得して生きて、最期を迎えられる世界を」をビジョンに掲げ、医療機関や薬局向けにオンライン診療やオンライン服薬指導サービスなどを提供するオンライン医療事業、医薬品の臨床開発向けのデジタルソリューション事業、デジタルセラピューティクス事業、保険事業等を展開しています。詳細については、https://micin.jp をご覧ください。
DCTプラットフォーム「MiROHA(ミロハ)」に関して
MICINが提供するDCTプラットフォーム「MiROHA」は、オンライン診療機能、eConsent機能、およびeSource(Electronic Source Data:臨床試験の原資料となり得る電子原データ)機能を搭載したDCTプラットフォームとして、2020年4月より提供を開始しています。現在、既に国内200以上の医療機関で4,000症例を越える患者さんに利用されています。これまで多くの製薬企業・医療機関に採用された実績をもとに、DCT領域のリーディングカンパニーとして、DCTシステムの提供だけでなく、新しくDCTに取り組まれる企業・医療機関への導入支援・コンサルテーションを積極的に行っています。
MiROHA ホームページ:https://www.miroha.co/
HERALD試験に関して
HERALD試験は、HER2遺伝子増幅が認められた固形がんに対するトラスツズマブデルクステカンの有効性と安全性を探索する臓器横断的医師主導治験です。主解析コホートは、リキッドバイオプシーにより患者スクリーニングを行いました(4)が、拡張コホートでは、保険診療でのがん遺伝子パネル検査(組織・血液)でHER2遺伝子増幅が認められた患者さんが対象となり、国内11施設を治験実施医療機関として行われています。
HERALD試験臨床試験情報:https://jrct.mhlw.go.jp/latest-detail/jRCT2080224635
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
- 種類
- その他
- ビジネスカテゴリ
- 医薬・製薬
- 関連リンク
- https://micin.jp/
- ダウンロード
