神経変性疾患治療薬の候補となる新規オートファジー誘導物質を同定
~オートファジー調節化合物の機能を統合的に解析する手法を開発~
順天堂大学大学院医学研究科オートファジー調節化合物探索研究講座の片浦哲志特任研究員、井本正哉特任教授、および神経学講座の斉木臣二准教授、服部信孝教授らの共同研究グループは、パーキンソン病(*1)などの神経変性疾患の新しい治療薬候補として期待される26種類のオートファジー(*2)誘導物質を同定しました。本研究では、ケミカルバイオロジー(*3)を用いてオートファジーの誘導メカニズムを推定する手法と、神経変性疾患に特徴的な細胞内の異常タンパク質凝集体除去活性を指標とした細胞実験系を組み合わせ、オートファジー誘導物質の機能を統合的に解析する手法を開発しました。本成果は、神経変性疾患の新しい治療薬候補を提示するとともに、オートファジーを利用した創薬研究の基盤形成を促進するものです。本論文は米国科学誌「Autophagy」誌のオンライン版に2020年8月7日付で公開されました。
本研究成果のポイント
背景
パーキンソン病はわが国でアルツハイマー病に次いで2番目に患者数の多い神経変性疾患で、2030年には全世界での患者数が1400万人を超えると推計されています。発症すると手足の震えやこわばりといった運動障害の症状が現れ徐々に進行していきますが、原因となる神経細胞死を抑制するような根本的治療薬の開発には未だ至っていません。今回、研究グループは、パーキンソン病の患者さんの脳神経細胞内に異常なタンパク質が凝集・蓄積していることに着目しました。異常なタンパク質は本来「オートファジー」という細胞の機能によって分解・除去されますが、パーキンソン病を含む複数の神経変性疾患ではオートファジーの機能が低下していることが分かりつつあります。そこで、研究グループは「オートファジーの機能を誘導し、異常なタンパク質の除去を促進する化合物」はパーキンソン病などの神経変性疾患の新しい治療薬になるのではないかと仮説を立て、研究を開始しました。
内容
これまでにオートファジーを誘導する様々な化合物が報告されています。これらの化合物の多くはパーキンソン病の治療薬の候補となることが期待される一方で、どのようなメカニズムでオートファジーを誘導するか、またオートファジーのどの過程に作用するかがわかっていないため、パーキンソン病の治療に、どの化合物が適しているかは不明でした。そこで本研究では、オートファジー活性の指標となる細胞内のタンパク質の量が、様々な化合物を加えることでどのように変化するかを調べる「ケミカルバイオロジー」の研究手法を用いて、化合物によるオートファジー誘導効果を分類することを試みました。
まずはじめに、さまざまなタンパク質の機能の阻害に関わるとされる400種類の化合物をスクリーニング(*4)し、39化合物をオートファジー誘導物質として同定しました。このうち、細胞毒性のない26化合物について、それらの作用をブロックする可能性のある200種類の化合物を用いて「ブロックされ方のパターン」により分類したところ、既にアルツハイマー型認知症薬として我が国でも使用されているメマンチンが、ER(小胞体)ストレスという仕組みを誘導することで、オートファジーを誘導して神経細胞を保護している可能性があることが分かりました。このことは本手法がオートファジーを誘導する化合物の作用機構解析に有用であることを示しています。
さらに今回の研究において特筆すべき成果は、この手法により、非常に珍しいオートファジー誘導メカニズムをもつSMK-17という化合物を見つけたことです。この化合物は過去に報告例の少ないPKC-TFEBという経路(*5)を活性化することでオートファジーを誘導することが証明されると共に、パーキンソン病やハンチントン病(*6)のモデル細胞の実験で、十分な薬効を示しました。すなわちパーキンソン病とハンチントン病のモデル細胞では、患者さんの脳内と同様に異常なタンパク質の凝集体が蓄積し、最終的に神経細胞死が起こりますが,ここにSMK-17を加えると細胞内の凝集タンパク質が綺麗に分解され、さらにパーキンソン病モデル細胞については神経細胞死も抑制できることが分かりました(図1)。これは、パーキンソン病やハンチントン病を発症し、すでに神経細胞内に異常なタンパク質が蓄積してしまった後でも、SMK-17を投与することで異常タンパク質を除去できる可能性を示唆しています。
今後の展開
多くの遺伝性パーキンソン病患者さんの原因遺伝子の機能を調べる研究から、パーキンソン病の病態はミトコンドリア機能が低下すること、異常なタンパク質の除去がうまく行われないことに集約されつつあります。研究グループが今回新たにオートファジー誘導物質として発見したSMK-17は、実験で人為的にミトコンドリア機能を低下させた場合に生じる異常なタンパク質をオートファジーにより除去するという結果が得られています。現在、SMK-17については新規治療薬の候補として実験動物を用いた評価を進めています。本研究手法で同定した26化合物が新規治療薬として確立されれば、オートファジーを利用した創薬研究の基盤形成を促進することにつながり、パーキンソン病やハンチントン病などの神経変性疾患に罹患されている多くの患者さんの病状を進行させないようにすることができると期待されます。
用語解説
*1 パーキンソン病:中脳黒質神経細胞脱落を特徴とする進行性の神経変性疾患。患者数は日本で推計14万人。
*2 オートファジー: 細胞内のタンパク質分解機構の一種。細胞・個体の恒常性維持に必要不可欠な細胞機能。
*3 ケミカルバイオロジー: 化合物を用いて生命現象を解析する研究分野。創薬研究への展開が容易な点からも期待される研究分野である。
*4 スクリーニング: 本研究では、大量の化合物の中から目的の活性を有する化合物のみを選別すること。
*5 PKC-TFEB経路: オートファジー関連遺伝子の発現を制御する転写因子TFEBがプロテインキナーゼC(PKC)によって活性化される経路。TFEBは通常mTOR経路により制御されているが、SMK-17はmTORに非依存的なPKCを介してTFEBを活性化させた。
*6 ハンチントン病: 舞踏運動などの不随意運動を主症状とする遺伝性の神経変性疾患。
原著論文
本研究は米国科学誌「Autophagy」のオンライン版で(2020年8月7日付)先行されました。
タイトル: A chemical genomics-aggrephagy integrated method studying functional analysis of autophagy inducers
タイトル(日本語訳):ケミカルゲノミクス・アグリファジー活性に基づくオートファジー誘導剤の統合的機能解析
著者: Tetsushi Kataura, Etsu Tashiro, Shota Nishikawa, Kensuke Shibahara, Yoshihito Muraoka, Masahiro Miura, Shun Sakai, Naohiro Katoh, Misato Totsuka, Masafumi Onodera, Kazuo Shin-ya, Kengo Miyamoto, Yukiko Sasazawa, Nobutaka Hattori, Shinji Saiki, Masaya Imoto
著者(日本語表記): 片浦哲志1,2,†、田代 悦1,††、西川将太1 、柴原健輔1 、村岡慶人1 、三浦昌大1 、酒井駿1 、加藤直裕1 、戸塚美里1 、小野寺雅史3 、新家一男4,5,6 、宮本健吾7 、吉川(笹澤)有紀子1,7 、服部信孝7 、斉木臣二7 、井本正哉1,†,†††
著者所属:1)慶應義塾大学理工学部生命情報学科、2)日本学術振興会特別研究員、 3)国立成育医療研究センター成育遺伝研究部、4)産業技術総合研究所創薬基盤研究部門、5)東京大学生物生産工学研究センター、6)東京大学微生物科学イノベーション連携研究機構、7)順天堂大学医学研究科神経学講座、†)現所属:順天堂大学医学研究科神経学講座、 ††)現所属: 昭和薬科大学薬学部生化学研究室、 †††)現所属:順天堂大学大学院医学研究科共同研究講座「オートファジー調節化合物探索研究講座」
DOI: 10.1080/15548627.2020.1794590
リンク先: http://dx.doi.org/10.1080/15548627.2020.1794590
本研究はJSPS科研費(研究代表者: 井本正哉:JP18H02099;斉木臣二:JP18KK0242, JP18KT0027;片浦哲志: JP19J12969)および文部科学省新学術領域研究学術研究支援基盤形成「先端モデル動物支援プラットフォーム」 JSPS科研費JP16H06276 (AdAMS) の支援を受け実施しました。また、オートファジーの測定に際し「GFP-LC3-RFPプローブ」をご供与下さいました東京大学大学院医学研究科 水島昇教授に御礼申し上げます。
なお、本研究にご協力いただいた皆様には深謝いたします。
- 神経変性疾患治療薬の候補となるオートファジー誘導物質26種類を同定
- オートファジー誘導物質の機能を統合的に解析する手法を開発
- 本手法によりオートファジーを利用した創薬研究の基盤形成を促進
背景
パーキンソン病はわが国でアルツハイマー病に次いで2番目に患者数の多い神経変性疾患で、2030年には全世界での患者数が1400万人を超えると推計されています。発症すると手足の震えやこわばりといった運動障害の症状が現れ徐々に進行していきますが、原因となる神経細胞死を抑制するような根本的治療薬の開発には未だ至っていません。今回、研究グループは、パーキンソン病の患者さんの脳神経細胞内に異常なタンパク質が凝集・蓄積していることに着目しました。異常なタンパク質は本来「オートファジー」という細胞の機能によって分解・除去されますが、パーキンソン病を含む複数の神経変性疾患ではオートファジーの機能が低下していることが分かりつつあります。そこで、研究グループは「オートファジーの機能を誘導し、異常なタンパク質の除去を促進する化合物」はパーキンソン病などの神経変性疾患の新しい治療薬になるのではないかと仮説を立て、研究を開始しました。
内容
これまでにオートファジーを誘導する様々な化合物が報告されています。これらの化合物の多くはパーキンソン病の治療薬の候補となることが期待される一方で、どのようなメカニズムでオートファジーを誘導するか、またオートファジーのどの過程に作用するかがわかっていないため、パーキンソン病の治療に、どの化合物が適しているかは不明でした。そこで本研究では、オートファジー活性の指標となる細胞内のタンパク質の量が、様々な化合物を加えることでどのように変化するかを調べる「ケミカルバイオロジー」の研究手法を用いて、化合物によるオートファジー誘導効果を分類することを試みました。
まずはじめに、さまざまなタンパク質の機能の阻害に関わるとされる400種類の化合物をスクリーニング(*4)し、39化合物をオートファジー誘導物質として同定しました。このうち、細胞毒性のない26化合物について、それらの作用をブロックする可能性のある200種類の化合物を用いて「ブロックされ方のパターン」により分類したところ、既にアルツハイマー型認知症薬として我が国でも使用されているメマンチンが、ER(小胞体)ストレスという仕組みを誘導することで、オートファジーを誘導して神経細胞を保護している可能性があることが分かりました。このことは本手法がオートファジーを誘導する化合物の作用機構解析に有用であることを示しています。
さらに今回の研究において特筆すべき成果は、この手法により、非常に珍しいオートファジー誘導メカニズムをもつSMK-17という化合物を見つけたことです。この化合物は過去に報告例の少ないPKC-TFEBという経路(*5)を活性化することでオートファジーを誘導することが証明されると共に、パーキンソン病やハンチントン病(*6)のモデル細胞の実験で、十分な薬効を示しました。すなわちパーキンソン病とハンチントン病のモデル細胞では、患者さんの脳内と同様に異常なタンパク質の凝集体が蓄積し、最終的に神経細胞死が起こりますが,ここにSMK-17を加えると細胞内の凝集タンパク質が綺麗に分解され、さらにパーキンソン病モデル細胞については神経細胞死も抑制できることが分かりました(図1)。これは、パーキンソン病やハンチントン病を発症し、すでに神経細胞内に異常なタンパク質が蓄積してしまった後でも、SMK-17を投与することで異常タンパク質を除去できる可能性を示唆しています。
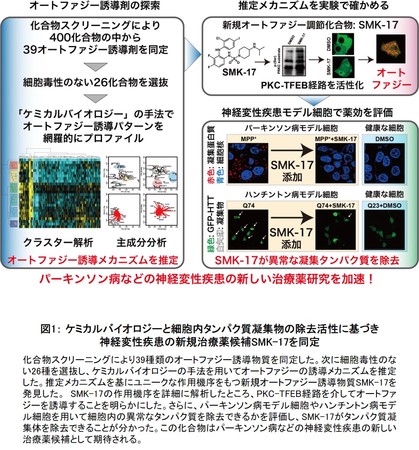 図1: ケミカルバイオロジーと細胞内タンパク質凝集物の除去活性に基づき神経変性疾患の新規治療薬候補SMK-17を同定
図1: ケミカルバイオロジーと細胞内タンパク質凝集物の除去活性に基づき神経変性疾患の新規治療薬候補SMK-17を同定
今後の展開
多くの遺伝性パーキンソン病患者さんの原因遺伝子の機能を調べる研究から、パーキンソン病の病態はミトコンドリア機能が低下すること、異常なタンパク質の除去がうまく行われないことに集約されつつあります。研究グループが今回新たにオートファジー誘導物質として発見したSMK-17は、実験で人為的にミトコンドリア機能を低下させた場合に生じる異常なタンパク質をオートファジーにより除去するという結果が得られています。現在、SMK-17については新規治療薬の候補として実験動物を用いた評価を進めています。本研究手法で同定した26化合物が新規治療薬として確立されれば、オートファジーを利用した創薬研究の基盤形成を促進することにつながり、パーキンソン病やハンチントン病などの神経変性疾患に罹患されている多くの患者さんの病状を進行させないようにすることができると期待されます。
用語解説
*1 パーキンソン病:中脳黒質神経細胞脱落を特徴とする進行性の神経変性疾患。患者数は日本で推計14万人。
*2 オートファジー: 細胞内のタンパク質分解機構の一種。細胞・個体の恒常性維持に必要不可欠な細胞機能。
*3 ケミカルバイオロジー: 化合物を用いて生命現象を解析する研究分野。創薬研究への展開が容易な点からも期待される研究分野である。
*4 スクリーニング: 本研究では、大量の化合物の中から目的の活性を有する化合物のみを選別すること。
*5 PKC-TFEB経路: オートファジー関連遺伝子の発現を制御する転写因子TFEBがプロテインキナーゼC(PKC)によって活性化される経路。TFEBは通常mTOR経路により制御されているが、SMK-17はmTORに非依存的なPKCを介してTFEBを活性化させた。
*6 ハンチントン病: 舞踏運動などの不随意運動を主症状とする遺伝性の神経変性疾患。
原著論文
本研究は米国科学誌「Autophagy」のオンライン版で(2020年8月7日付)先行されました。
タイトル: A chemical genomics-aggrephagy integrated method studying functional analysis of autophagy inducers
タイトル(日本語訳):ケミカルゲノミクス・アグリファジー活性に基づくオートファジー誘導剤の統合的機能解析
著者: Tetsushi Kataura, Etsu Tashiro, Shota Nishikawa, Kensuke Shibahara, Yoshihito Muraoka, Masahiro Miura, Shun Sakai, Naohiro Katoh, Misato Totsuka, Masafumi Onodera, Kazuo Shin-ya, Kengo Miyamoto, Yukiko Sasazawa, Nobutaka Hattori, Shinji Saiki, Masaya Imoto
著者(日本語表記): 片浦哲志1,2,†、田代 悦1,††、西川将太1 、柴原健輔1 、村岡慶人1 、三浦昌大1 、酒井駿1 、加藤直裕1 、戸塚美里1 、小野寺雅史3 、新家一男4,5,6 、宮本健吾7 、吉川(笹澤)有紀子1,7 、服部信孝7 、斉木臣二7 、井本正哉1,†,†††
著者所属:1)慶應義塾大学理工学部生命情報学科、2)日本学術振興会特別研究員、 3)国立成育医療研究センター成育遺伝研究部、4)産業技術総合研究所創薬基盤研究部門、5)東京大学生物生産工学研究センター、6)東京大学微生物科学イノベーション連携研究機構、7)順天堂大学医学研究科神経学講座、†)現所属:順天堂大学医学研究科神経学講座、 ††)現所属: 昭和薬科大学薬学部生化学研究室、 †††)現所属:順天堂大学大学院医学研究科共同研究講座「オートファジー調節化合物探索研究講座」
DOI: 10.1080/15548627.2020.1794590
リンク先: http://dx.doi.org/10.1080/15548627.2020.1794590
本研究はJSPS科研費(研究代表者: 井本正哉:JP18H02099;斉木臣二:JP18KK0242, JP18KT0027;片浦哲志: JP19J12969)および文部科学省新学術領域研究学術研究支援基盤形成「先端モデル動物支援プラットフォーム」 JSPS科研費JP16H06276 (AdAMS) の支援を受け実施しました。また、オートファジーの測定に際し「GFP-LC3-RFPプローブ」をご供与下さいました東京大学大学院医学研究科 水島昇教授に御礼申し上げます。
なお、本研究にご協力いただいた皆様には深謝いたします。
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザーログイン既に登録済みの方はこちら
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
- 種類
- その他
- ダウンロード
