ミトコンドリアが細胞に取り込まれるメカニズムを解明 ~細胞のエネルギー機能を直接補う次世代医療の実現に大きく前進~
【研究の要旨とポイント】
次世代治療として注目されているミトコンドリア移植療法において、ミトコンドリアが能動的に細胞に取り込まれるプロセスを定量的、機構的に実証しました。
ミトコンドリアは複数のエンドサイトーシス経路を介して段階的に取り込まれ、取り込まれた後も機能を維持することを明らかにしました。
細胞のエネルギー機能を直接補うミトコンドリア移植療法の実現に向けた基盤となる成果です。
【研究の概要】
東京理科大学 薬学部 生命創薬科学科の草森 浩輔准教授、後藤 雅弥氏(薬学部5年)、同大学 薬学部 薬学科の西川 元也教授、板倉 祥子助教、金井 舞氏(博士課程4年)らの研究グループは、次世代治療法として注目される「ミトコンドリア移植療法」において、細胞がミトコンドリアを取り込み、機能を発現させるメカニズムを定量的・機構的に解明しました。
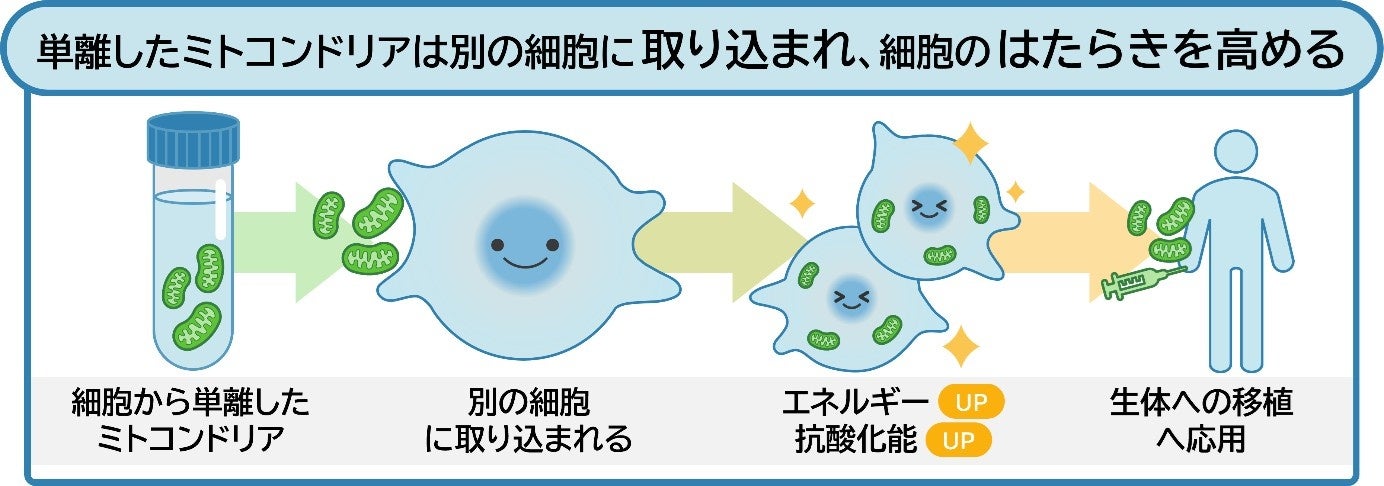
ミトコンドリアは、細胞内でエネルギー産生などの重要な機能を担う細胞小器官であり、その機能が損なわれるとさまざまな疾患の発症につながります。ミトコンドリア移植療法は、単離したミトコンドリアを投与することで細胞機能を改善する治療法で、これまで治療が難しかった疾患に適用できると期待されています。しかし、この治療法においてミトコンドリアが実際にどのように細胞内に取り込まれ、機能するのかといったメカニズムは不明でした。
本研究では、間葉系間質細胞(mesenchymal stromal cell:MSC、*1)から機能的なミトコンドリアを単離し、その性質や細胞への影響を詳細に解析しました。その結果、ミトコンドリアをMSCに添加すると細胞の増殖が促進され、ストレス環境下での生存性が向上し、エネルギー産生能が高まることが確認されました。
また、蛍光イメージングによりミトコンドリアが時間とともに細胞へ取り込まれる様子を可視化し、6時間以内に取り込まれることを明らかにしました。さらに、エンドサイトーシス(*2)を抑制する薬剤を添加するとミトコンドリアの取り込みが阻害されたことから、細胞内への取り込みは主にエネルギー依存的な経路を介することがわかりました。
本研究は、ミトコンドリアが細胞に取り込まれた後も機能を保持し、細胞機能を改善することを示した重要な成果です。今回の知見はミトコンドリア移植を基盤とした新たな治療法開発に向けた科学的基盤を提供します。
本研究成果は、2025年12月29日に国際学術誌「Scientific Reports」にオンライン掲載されました。
【研究の背景】
ミトコンドリアはATP産生(*3)を通じた細胞のエネルギー代謝に加え、活性酸素種の制御、脂質代謝など多様な機能を持つ重要な細胞小器官です。その機能不全は神経変性疾患、虚血再灌流障害、代謝性疾患など、様々な疾患の病因に関与しています。
近年、単離したミトコンドリアを投与する「ミトコンドリア移植療法」が注目されており、心筋梗塞、肝不全、神経疾患などの前臨床モデルで有益な効果が報告されています。
しかし、これらの治療効果の細胞学的基盤は不明確でした。ミトコンドリアが実際に細胞内に取り込まれているという実験的な証拠は限定的であり、そのメカニズムはほとんど解明されていませんでした。また、取り込まれたミトコンドリアが細胞にどのような影響を及ぼすかも不明でした。
そこで本研究グループは、間葉系間質細胞(MSC)から機能的なミトコンドリアを単離し、その特性や細胞への影響、取り込みメカニズムについて詳細に解析しました。
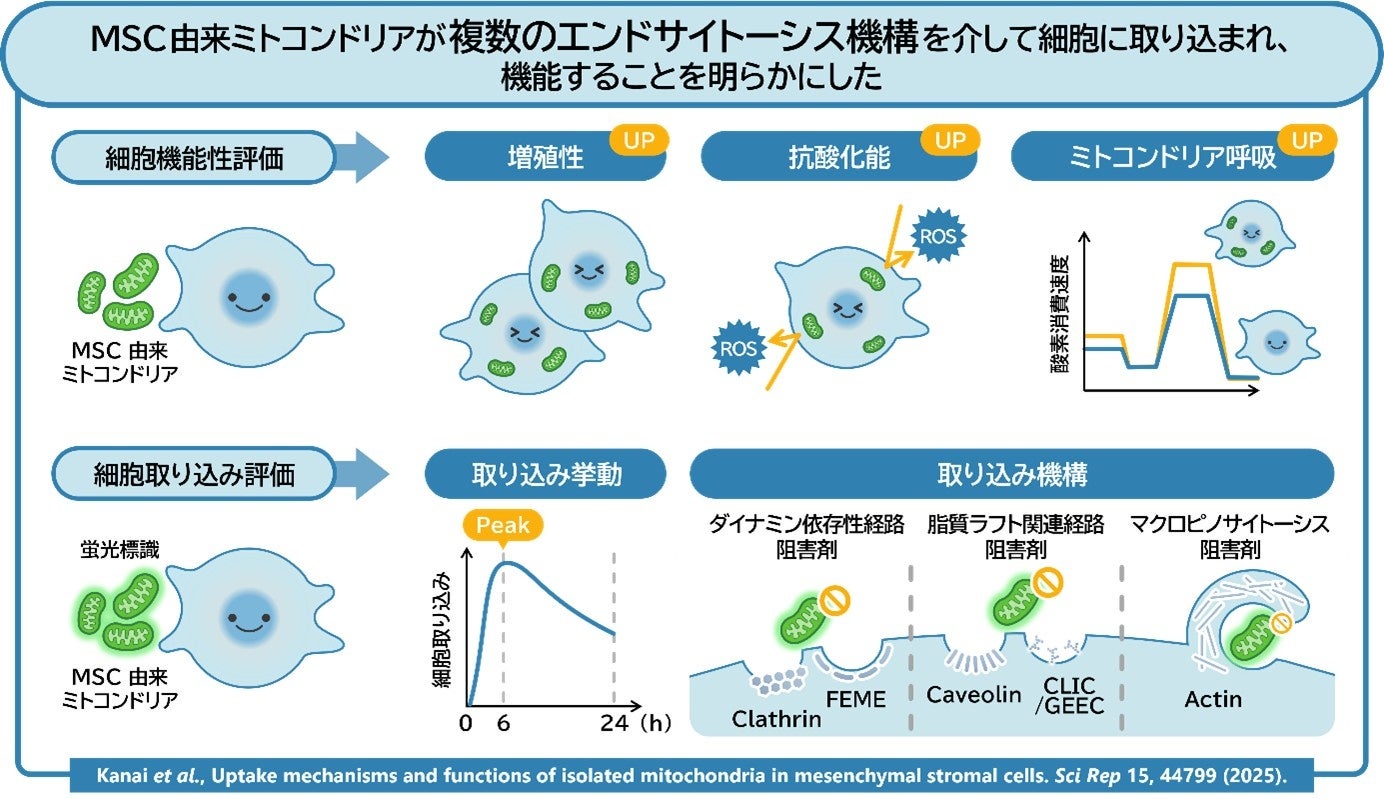
図. 間葉系間質細胞から単離したミトコンドリアの機能性と細胞取り込み評価。
MSCミトコンドリア添加後の細胞では、細胞増殖性、ミトコンドリア呼吸(酸素消費速度)、および活性酸素に対する抗酸化能の向上が観察された(上)。緑色蛍光色素で標識したMSCの細胞取り込み量は0.5時間後から増加し、6時間で最大となった。阻害剤を用いた解析から、ダイナミン依存性経路、脂質ラフト関連経路、マクロピノサイトーシスなど、複数のエンドサイトーシス機構が取り込みに関与することが示唆された(下)。
MSC, mesenchymal stromal cell(間葉系間質細胞); ROS, reactive oxygen species(活性酸素種); FEME, fast endophilin-mediated endocytosis; CLIC/GEEC, clathrin-independent carriers/GPI-enriched endocytic compartments.
【研究結果の詳細】
研究グループはまず、マウスの間葉系間質細胞株(MSC)からミトコンドリアを単離し、動的光散乱(DLS)分析により、平均直径は1,000 nm、ゼータ電位16 mVの純度の高い均一粒子であることを確認しました。また、ATP量測定の結果、代謝活性を維持していることが確認されました。
単離されたミトコンドリアを別のMSCに添加し、観察すると濃度依存的な細胞増殖の促進が確認されました。また、肝細胞傷害モデルでは肝細胞保護効果が確認されました。酸素消費速度(OCR)測定により、添加した細胞では基礎呼吸速度、ATP産生速度、最大呼吸能がいずれも濃度依存的に増加することが明らかになりました。
次に、ミトコンドリアに蛍光標識を施し、MSCに添加して観察したところ、0.5時間後から細胞内への蓄積が始まり、6時間後に顕著に細胞内局在を確認できました。フローサイトメトリーによる定量解析でも同様に、蛍光強度は時間依存的に増加し、6時間後にピークに達しました。また、光波動場三次元顕微鏡を用いて非標識でミトコンドリアを観察したところ、同様にミトコンドリアの段階的な細胞取り込みが確認されました。
ミトコンドリアの取り込みメカニズムを解明するため、低温培養とエンドサイトーシス阻害剤を用いた実験を行いました。4Cの培養では37Cと比較して取り込みは著しく減少し、エネルギー依存的な取り込みであることが明らかになりました。
さらに、エンドサイトーシス阻害剤で前処理をしたところ、取り込みは有意に減少しました。メチル-β-シクロデキストリンをはじめとする各種エンドサイトーシス阻害剤を利用した検討により顕著な取り込みの減少が見られたことから、MSCは複数のエンドサイトーシス経路を介して単離ミトコンドリアを能動的に取り込むことが明らかになりました。
本研究により、ミトコンドリアがMSCに能動的に取り込まれ、細胞内で機能を保持することが定量的・機構的に実証されました。この知見は、ミトコンドリア移植療法の細胞学的基盤を確立するものです。研究を主導した草森准教授は「ミトコンドリアを疾患治療に利⽤するという未知に大きな興味を持ち、本研究に取り組みました。今後、細胞のエネルギー機能を直接補うミトコンドリア治療という新しい医療の道が開かれ、心筋梗塞、脳卒中、肝疾患、神経変性疾患など、ミトコンドリア機能不全が関与する様々な疾患に対する、より安全で持続可能な治療法の実現に貢献することが期待されます」とコメントしています。
-
本研究は、日本学術振興会(JSPS)の科学研究費助成事業 基盤研究(B)(23H03749、23K28437)、挑戦的研究(萌芽)(23K18595)、キヤノン財団、Leading Pioneers Science Foundation、文部科学省(MEXT)および科学技術振興機構(JST)による Greater Tokyo Innovation Ecosystem(GTIE)の助成を受けて実施したものです。
【用語】
*1 間葉系間質細胞:MSC
間葉系間質細胞(MSC:mesenchymal stromal cell)のこと。細胞医薬としても応用されており、多様な細胞に分化する幹細胞様の機能や特性を有する。
*2 エンドサイトーシス
細胞が外部の物質を細胞内に取り込むメカニズム。取り込みに関わる分子機構の違いにより、複数の経路がある。エネルギーを必要とする能動的な過程。
*3 ATP産生
アデノシン三リン酸(adenosine triphosphate:ATP)の産生。ATPは細胞のエネルギー通貨として機能する分子であり、ミトコンドリアが酸化的リン酸化を通じて産生する。
【論文情報】

|
雑誌名 |
:Scientific Reports |
|
論文タイトル |
:Uptake mechanisms and functions of isolated mitochondria in mesenchymal stromal cells |
|
著者 |
:Mai Kanai, Miyabi Goto, Shoko Itakura, Makiya Nishikawa, Kosuke Kusamori |
|
DOI |
※PR TIMESのシステムでは上付き・下付き文字や特殊文字等を使用できないため、正式な表記と異なる場合がございますのでご留意ください。正式な表記は、東京理科大学WEBページ(https://www.tus.ac.jp/today/archive/20260303_5527.html)をご参照ください。
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
