白血病細胞は周囲の細胞からミトコンドリアを受け取り生き残る
~ 抗がん剤治療後の再発を防ぐ治療法の開発へ期待 ~
順天堂大学大学院医学研究科・臨床病態検査医学の田部陽子 教授、齋藤香里 研究員らと米国 MD Anderson がんセンターのMarina Konopleva 教授らは国際共同研究により、白血病細胞が周囲の細胞に働きかけることで自らのミトコンドリアの機能を回復させることを明らかにしました。今回の研究では、ミトコンドリアでの呼吸が阻害され白血病細胞が、周囲の細胞から直接ミトコンドリアを受け取ることや、自身のミトコンドリアの分裂を促進させて機能を高めることにより、生存に必要なエネルギーを作り出すことを発見しました。本研究により抗がん剤治療後に骨髄の中に残存する白血病細胞がエネルギーを得る仕組みを明らかにしたことで、このプロセスを阻止する新たな治療戦略が立てられるようになり、白血病の再発を阻止する治療法の開発に役立てられることが期待されます。本研究は、米国の学術雑誌「Blood Advances」のオンライン版に掲載されました。
本研究成果のポイント
背景
白血病は血液や骨髄の中に腫瘍細胞(白血病細胞)が出現する病気です。白血病細胞は、骨髄の中の特異な環境(骨髄微小環境)で、限られた栄養素や酸素量に適応しながら生存し、増殖していきます。この白血病細胞は、細胞内小器官であるミトコンドリアでの呼吸(酸化的リン酸化、OxPhos)によって生存に必要なエネルギーを得ていることから、白血病治療ではミトコンドリア呼吸の阻害剤を用いる戦略が考えられます。しかしながら、その際、骨髄微小環境で周囲の間質細胞との相互作用により白血病細胞が生き残り、治療後の再発の原因になるという課題がありました。そこで本研究では、白血病細胞がミトコンドリア呼吸を阻害されるストレスにさらされた際に、周囲の細胞にどのように働きかけて、どのような仕組みでミトコンドリア機能を維持しエネルギーを得て生き残るのかを明らかにする目的で行いました。
内容
まず、白血病細胞と骨髄に存在する間質細胞との直接的な相互作用について調べました。研究チームが以前の研究で見出した細胞内のミトコンドリア呼吸鎖複合体Ⅰ(*4)に対する阻害剤を使用して、間質細胞と共培養した白血病細胞での酸素消費率や細胞死の変化を調べとともに、共焦点顕微鏡や電子顕微鏡によるイメージング解析を行いました。また、マウス実験を用いて生体内での白血病細胞の遺伝子発現の変化を調べました。その結果、ミトコンドリア呼吸を阻害された白血病細胞は、突起を出しながら骨髄間質細胞に向かって移動し、トンネルナノチューブを形成し、これを介して間質細胞からミトコンドリアを受け取るという現象を発見しました(図1) 。
以上の結果から、骨髄微小環境で生じるエネルギー欠乏状態において、白血病細胞は周囲の細胞から直接ミトコンドリアを受け取るとともに、自身のミトコンドリアの分裂を促進させて機能を高めることにより生存に必要なエネルギーを作り出すことがわかりました。
今後の展開
本研究により、今まで不明であった白血病細胞が抗がん剤から生き残る仕組みを明らかにしました。白血病細胞は、骨髄微小環境内の白血病細胞が周囲の細胞から直接的にミトコンドリアを受け取り、また、自らのミトコンドリアの分裂能を高めることによってミトコンドリア呼吸の阻害に抵抗性を強め、生存に必要なエネルギーを得ていることから、腫瘍細胞が周囲の細胞を利用してエネルギー枯渇を代償するプロセスを阻止することで、様々な治療薬の抗腫瘍効力を高める効果があると考えられます。本成果は、白血病の再発防止の治療法の開発のみならず、今後のがん代謝制御治療に役立つことが期待されます。
用語解説
*1 ミトコンドリア呼吸: ミトコンドリアは細胞内にある小器官で、酸素を用いた呼吸によって一連のリン酸化を行い、効率的にエネルギーを産生する。
*2 トンネルナノチューブ: 細胞膜から突出する長くて細い管で、異なる細胞を接続する。ミトコンドリアなどがトンネルナノチューブを介して細胞間で輸送される。
*3 マイトファジー: 機能不全を起こしたミトコンドリアを自食作用(オートファジー)で分解する機能。
*4 ミトコンドリア呼吸鎖複合体Ⅰ:ミトコンドリアの内膜上にはⅠ~Ⅳまでの4つの呼吸鎖複合体があり、エネルギー産生に酸化還元反応を利用している。
原著論文
本研究成果は、米国の学術雑誌「Blood Advances」のオンライン版に掲載(2021年9月10日)されました。
論文タイトル: Exogenous mitochondrial transfer and endogenous mitochondrial fission facilitate AML resistance to OxPhos inhibition
日本語訳: 白血病細胞の酸化的リン酸化阻害抵抗性に寄与するミトコンドリア機能回復
著者:Kaori Saito(齋藤香里) 1, Qi Zhang 2, Haeun Yang(梁夏恩) 1, Kotoko Yamatani(山谷琴子) 1, Tomohiko Ai(藍智彦) 1, Vivian Ruvolo 2, Natalia Baran 2, Tianyu Cai 2, Helen Ma 2, Rodrigo Jacamo 2, Vinitha Kuruvilla 2, Junichi Imoto(井元順一) 4, Sonoko Kinjo(金城その子) 4, Kazuho Ikeo(池尾一穂) 4, Kaori Moriya(守屋香織) 3, Koya Suzuki(鈴木浩也) 1, Takashi Miida(三井田孝) 1, Yong-Mi Kim, Christopher P. Vellano 2, Michael Andreeff 2, Joseph R. Marszalek 2, Yoko Tabe(田部陽子) 1, 2, Marina Konopleva 2
所属機関(日本語表記): 順天堂大学大学院医学研究科臨床病態検査医学1、米国MDアンダーソンがんセンター2、順天堂大学大学院医学研究科研究基盤センター生体分子研究室3、国立遺伝学研究所4
DOI: 10.1182/bloodadvances.2020003661
本研究は、本論文は、順天堂大学と米国MDアンダーソンがんセンターの間で取り交わされた姉妹協定に基づく共同研究のひとつとして取り組んできた国際共同研究の成果で、JSPS科研費(基盤研究C JP18K07424)、高松宮妃癌研究基金研究助成金、ならびに日本白血病研究基金 クレディセゾン賞の支援を受け実施されました。
- ミトコンドリア呼吸(*1)が阻害された白血病細胞がトンネルナノチューブ(*2)を介して骨髄微小環境に存在する周囲の細胞から直接ミトコンドリアを取り込むことを発見
- 同時に白血病細胞内でミトコンドリアの分裂の進行と機能の衰えたミトコンドリアの排除(マイトファジー*3)が生じることを発見
- ミトコンドリア機能の向上と回復をもたらすこれらのプロセスが、白血病の再発を阻止するための新たな標的になると期待される
背景
白血病は血液や骨髄の中に腫瘍細胞(白血病細胞)が出現する病気です。白血病細胞は、骨髄の中の特異な環境(骨髄微小環境)で、限られた栄養素や酸素量に適応しながら生存し、増殖していきます。この白血病細胞は、細胞内小器官であるミトコンドリアでの呼吸(酸化的リン酸化、OxPhos)によって生存に必要なエネルギーを得ていることから、白血病治療ではミトコンドリア呼吸の阻害剤を用いる戦略が考えられます。しかしながら、その際、骨髄微小環境で周囲の間質細胞との相互作用により白血病細胞が生き残り、治療後の再発の原因になるという課題がありました。そこで本研究では、白血病細胞がミトコンドリア呼吸を阻害されるストレスにさらされた際に、周囲の細胞にどのように働きかけて、どのような仕組みでミトコンドリア機能を維持しエネルギーを得て生き残るのかを明らかにする目的で行いました。
内容
まず、白血病細胞と骨髄に存在する間質細胞との直接的な相互作用について調べました。研究チームが以前の研究で見出した細胞内のミトコンドリア呼吸鎖複合体Ⅰ(*4)に対する阻害剤を使用して、間質細胞と共培養した白血病細胞での酸素消費率や細胞死の変化を調べとともに、共焦点顕微鏡や電子顕微鏡によるイメージング解析を行いました。また、マウス実験を用いて生体内での白血病細胞の遺伝子発現の変化を調べました。その結果、ミトコンドリア呼吸を阻害された白血病細胞は、突起を出しながら骨髄間質細胞に向かって移動し、トンネルナノチューブを形成し、これを介して間質細胞からミトコンドリアを受け取るという現象を発見しました(図1) 。
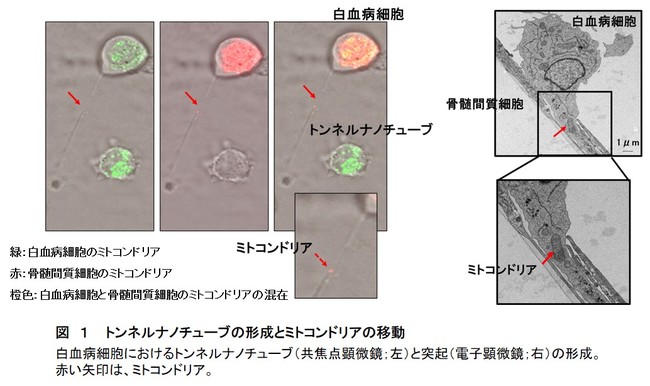 図 1 トンネルナノチューブの形成とミトコンドリアの移動
図 1 トンネルナノチューブの形成とミトコンドリアの移動
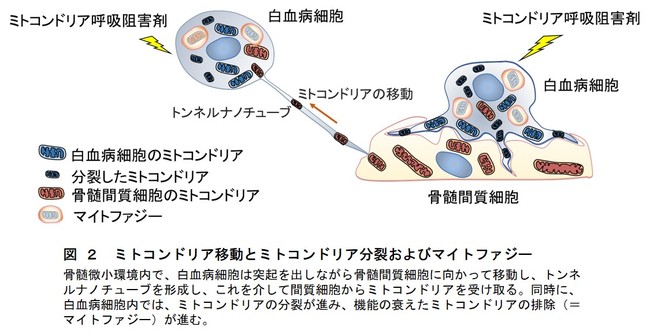 図 2 ミトコンドリア移動とミトコンドリア分裂およびマイトファジー
図 2 ミトコンドリア移動とミトコンドリア分裂およびマイトファジー
以上の結果から、骨髄微小環境で生じるエネルギー欠乏状態において、白血病細胞は周囲の細胞から直接ミトコンドリアを受け取るとともに、自身のミトコンドリアの分裂を促進させて機能を高めることにより生存に必要なエネルギーを作り出すことがわかりました。
今後の展開
本研究により、今まで不明であった白血病細胞が抗がん剤から生き残る仕組みを明らかにしました。白血病細胞は、骨髄微小環境内の白血病細胞が周囲の細胞から直接的にミトコンドリアを受け取り、また、自らのミトコンドリアの分裂能を高めることによってミトコンドリア呼吸の阻害に抵抗性を強め、生存に必要なエネルギーを得ていることから、腫瘍細胞が周囲の細胞を利用してエネルギー枯渇を代償するプロセスを阻止することで、様々な治療薬の抗腫瘍効力を高める効果があると考えられます。本成果は、白血病の再発防止の治療法の開発のみならず、今後のがん代謝制御治療に役立つことが期待されます。
用語解説
*1 ミトコンドリア呼吸: ミトコンドリアは細胞内にある小器官で、酸素を用いた呼吸によって一連のリン酸化を行い、効率的にエネルギーを産生する。
*2 トンネルナノチューブ: 細胞膜から突出する長くて細い管で、異なる細胞を接続する。ミトコンドリアなどがトンネルナノチューブを介して細胞間で輸送される。
*3 マイトファジー: 機能不全を起こしたミトコンドリアを自食作用(オートファジー)で分解する機能。
*4 ミトコンドリア呼吸鎖複合体Ⅰ:ミトコンドリアの内膜上にはⅠ~Ⅳまでの4つの呼吸鎖複合体があり、エネルギー産生に酸化還元反応を利用している。
原著論文
本研究成果は、米国の学術雑誌「Blood Advances」のオンライン版に掲載(2021年9月10日)されました。
論文タイトル: Exogenous mitochondrial transfer and endogenous mitochondrial fission facilitate AML resistance to OxPhos inhibition
日本語訳: 白血病細胞の酸化的リン酸化阻害抵抗性に寄与するミトコンドリア機能回復
著者:Kaori Saito(齋藤香里) 1, Qi Zhang 2, Haeun Yang(梁夏恩) 1, Kotoko Yamatani(山谷琴子) 1, Tomohiko Ai(藍智彦) 1, Vivian Ruvolo 2, Natalia Baran 2, Tianyu Cai 2, Helen Ma 2, Rodrigo Jacamo 2, Vinitha Kuruvilla 2, Junichi Imoto(井元順一) 4, Sonoko Kinjo(金城その子) 4, Kazuho Ikeo(池尾一穂) 4, Kaori Moriya(守屋香織) 3, Koya Suzuki(鈴木浩也) 1, Takashi Miida(三井田孝) 1, Yong-Mi Kim, Christopher P. Vellano 2, Michael Andreeff 2, Joseph R. Marszalek 2, Yoko Tabe(田部陽子) 1, 2, Marina Konopleva 2
所属機関(日本語表記): 順天堂大学大学院医学研究科臨床病態検査医学1、米国MDアンダーソンがんセンター2、順天堂大学大学院医学研究科研究基盤センター生体分子研究室3、国立遺伝学研究所4
DOI: 10.1182/bloodadvances.2020003661
本研究は、本論文は、順天堂大学と米国MDアンダーソンがんセンターの間で取り交わされた姉妹協定に基づく共同研究のひとつとして取り組んできた国際共同研究の成果で、JSPS科研費(基盤研究C JP18K07424)、高松宮妃癌研究基金研究助成金、ならびに日本白血病研究基金 クレディセゾン賞の支援を受け実施されました。
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザーログイン既に登録済みの方はこちら
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
