膵臓が細菌感染から腸を守る新たな機構を発見ー膵臓が腸の粘膜の第一線のバリアとして働くタンパク質を分泌ー
千葉大学大学院医学研究院イノベーション医学研究領域の倉島洋介准教授(東京大学医科学研究所臨床ワクチン学分野特任准教授)と東京大学医科学研究所粘膜免疫学部門の清野宏特任教授(カリフォルニア大学サンディエゴ校教授、千葉大学大学院医学研究院特任教授)らの研究グループは、食物の消化を担う臓器として知られる「膵(すい)臓」が細菌感染から腸管を守る働きを持つことを初めて明らかにしました。膵臓から大量に分泌される「Glycoprotein2:GP2(注1)」と呼ばれる糖タンパクが腸内細菌の表面(線毛)を捉えることで、組織中への移行を抑えていることを見出しました。この膵臓タンパク質の分泌が損なわれると、腸内細菌の組織中や血中への移行が起こりやすくなり、炎症性腸疾患の重症化につながることを発見しました(図1)。この成果はNature Communicationsに2月16日に掲載されました。
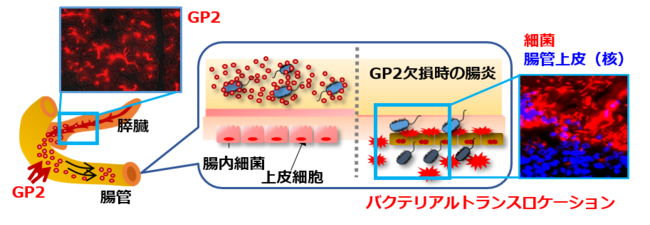 図1.膵臓から分泌されるGP2が細菌感染から体を防御する仕組み
図1.膵臓から分泌されるGP2が細菌感染から体を防御する仕組み
- 研究の背景
これまで、GP2の遺伝子変異が膵臓がんのリスクの上昇につながることや、GP2に反応をする自己抗体が炎症性腸疾患の患者では多く検出されることが報告されていましたが、膵臓から分泌されるGP2の役割はほとんど分かっていませんでした。
また、腸管の機能低下が多臓器不全を引き起こすメカニズムには、炎症性腸疾患などの消化管疾患や免疫能の低下、全身的な栄養不全、ストレス、細菌の異常増殖により、生きた腸内細菌が腸管内から粘膜組織や腸管のリンパ節、他の臓器へと移行・感染する「バクテリアルトランスロケーション」と呼ばれる現象が関与していると考えられています。この現象に対して生体内が持つ防御機構を調べることや、仕組みを紐解き、それを活用することでバクテリアルトランスロケーションによって悪化する多くの疾患に対する予防法や治療法への応用が可能であると考えられてきました。しかし、バクテリアルトランスロケーションが起こる明確な原因は分かっていませんでした。
- 研究成果
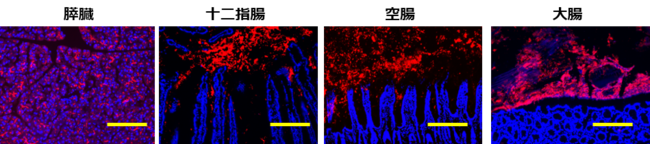 図2. 膵臓から分泌され腸管管腔に流れるGP2(GP2、組織細胞(核))スケールバー100mm
図2. 膵臓から分泌され腸管管腔に流れるGP2(GP2、組織細胞(核))スケールバー100mm
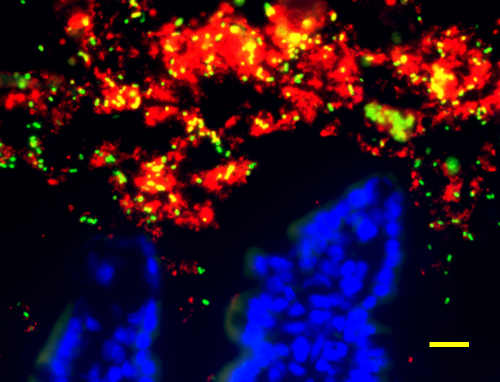 図3. 腸管管腔のGlycoprotein2と腸内細菌(GP2、腸内細菌、腸管絨毛(核))スケールバー20mm
図3. 腸管管腔のGlycoprotein2と腸内細菌(GP2、腸内細菌、腸管絨毛(核))スケールバー20mm
これらの結果から、腸管の上部に位置する膵臓の新 しい役割として、バクテリアルトランスロケーションや食物などからの細菌感染から体を守る粘膜の第一線のバリアとして働いていると考えられます。
- 今後の展望
- 研究者のコメント

- 用語解説
(注2)サイトカイン:主に免疫系細胞から分泌されるタンパク質で、標的となる細胞の表面に存在する特異的受容体に作用して細胞間の情報伝達を担う生理活性物質。
- 論文情報
発表者:Yosuke Kurashima, Takaaki Kigoshi, Sayuri Murasaki, Fujimi Arai, Kaoru Shimada, Natsumi Seki, Yun-Gi Kim, Koji Hase, Hiroshi Ohno, Kazuya Kawano, Hiroshi Ashida, Toshihiko Suzuki, Masako Morimoto, Yukari Saito, Ai Sasou, Yuki Goda, Yoshikazu Yuki, Yutaka Inagaki, Hideki Iijima, Wataru Suda, Masahira Hattori, and Hiroshi Kiyono
掲載誌:Nature Communications
DOI:https://doi.org/10.1038/s41467-021-21277-2
- 研究プロジェクトについて
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザーログイン既に登録済みの方はこちら
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
