新たなオートファジー経路を発見
― 革新的技術が明らかにした細胞の恒常性を維持する仕組み ―
本研究成果のポイント
オートファジーで分解されるたんぱく質を効率よく精製し同定する革新的手法を確立
巨大なたんぱく質複合体「ヴォルト」を分解する新規オートファジー経路(ヴォルトファジー)を発見
がんや神経変性疾患などオートファジー関連疾患の発症機序の解明につながる
背景
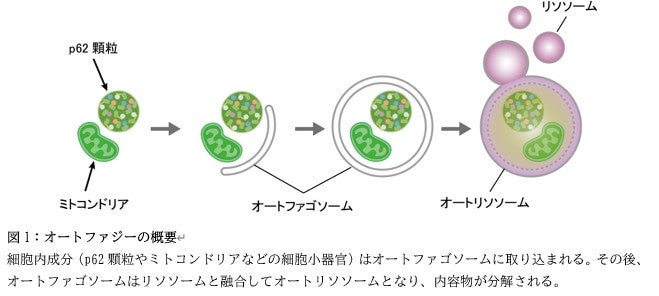
オートファジー(自食作用:細胞が自己成分を分解する機能)は、細胞内のたんぱく質や細胞小器官などをリソソームに輸送し、それらを分解する仕組みです(図1)。近年、オートファジーは細胞内を無作為に分解するだけでなく、細胞内の特定のたんぱく質を効率良く分解する作用を有することが明らかになり、この作用は「選択的オートファジー(*2)」と呼ばれています。選択的オートファジーの代表的な標的として知られているのが「p62顆粒(*3)」です。p62顆粒は、p62と呼ばれるたんぱく質とユビキチン化タンパク質などの他の様々なたんぱく質が液―液相分離(*4)して形成された、膜に包まれていない細胞小器官であり、p62顆粒の分解不全はがんや神経変性疾患の病態に関与すると考えられています。しかし、これまでp62顆粒に含まれるたんぱく質を同定する手法が存在しなかったため、p62顆粒の構成成分やその分解の意義は不明でした。
内容
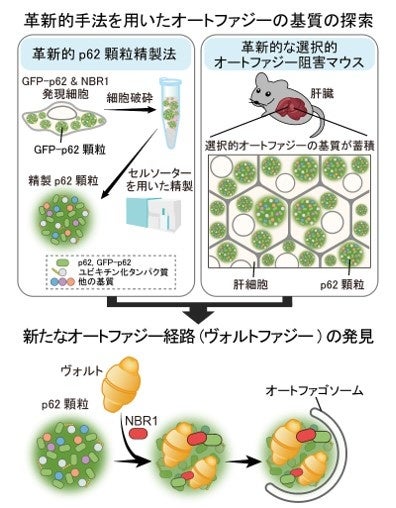
今回、研究グループはp62顆粒を介して選択的オートファジーで分解されるたんぱく質の同定を目的として、まず蛍光標識したp62顆粒をセルソーター(*5)を用いて効率よく精製する手法を確立しました(図2)。次に、精製したp62顆粒に含まれるたんぱく質を質量分析により網羅的に同定しました。さらに、革新的な選択的オートファジー阻害マウスの肝臓を用いて、選択的オートファジーで分解されるたんぱく質も網羅的に同定しました(図2)。これら二つの革新的手法で得られた結果を統合的に解析した結果、巨大なたんぱく質複合体ヴォルト(vault)(*6)がp62顆粒を介して選択的オートファジーで分解されるというこれまで全く知られていなかった新たなオートファジー経路を見出すことに成功し、この分解経路を「ヴォルトファジー(vault-phagy)」と名付けました(図2)。
この新たなオートファジー経路の意義を明らかにするため、p62顆粒の分解不全を伴う非アルコール性脂肪性肝炎(*7)由来のヒト肝細胞がん検体を解析した結果、肝細胞がんの腫瘍部において肝細胞内にヴォルトが蓄積していることを見出しました。さらにこの時ヴォルトは「マロリー・デンク体(*8)」と呼ばれるp62陽性構造体に集積していることもわかりました。これまでにヴォルトの蓄積は肝細胞がんを促進することが報告されていることから、以上の結果は、ヴォルトファジーの障害が肝細胞がんの発症に関連することを強く示唆しています。
以上の解析を通じて、細胞内の恒常性維持を担う新たな仕組みとして、細胞内の巨大なたんぱく質複合体ヴォルトを選択的に分解するオートファジー経路の存在が初めて明らかになりました。

今後の展開
これまでにオートファジーの異常は、がんや神経変性疾患などのオートファジー関連疾患の原因となることが示されています。今回研究グループが確立した手法は、これらの疾患の解析にも適応できることから、将来的にがんや神経変性疾患等の病態や発症機序の解明、そしてそれら疾患の治療につながることが期待されます。
用語解説
*1 細胞の恒常性: 細胞の内部や外部の環境因子の変化にかかわらず、細胞の状態が一定に保たれるという性質。健康を定義する重要な要素でもある。
*2 選択的オートファジー: 細胞内の特定のたんぱく質や細胞小器官(ミトコンドリアや小胞体など)を選択的にオートファゴソームに取り込み、リソソーム(分解酵素を格納している細胞小器官)で分解する作用。選択的オートファジーの異常はがんや神経変性疾患と関連すると考えられている。
*3 p62顆粒: 肝細胞がんや神経変性疾患の病変細胞では巨大な構造体であるp62顆粒を形成する。p62は、たんぱく質恒常性の破綻、酸化ストレス、あるいは炎症性ストレスなどにより発現誘導される多機能たんぱく質である。最も代表的なオートファジー選択的分解基質であり、ユビキチン化たんぱく質と結合することで液−液相分離を起こす。p62は転写因子Nrf2を負に制御するKeap1とも結合することが知られている。
*4 液―液相分離: 均一に混ざり合った溶液が、互いに溶け合わない二相に分離する現象。細胞内では、たんぱく質や核酸同士の弱い相互作用によって起こることが知られている。ミトコンドリアなどの膜で包まれた細胞小器官は膜によって区切られることで区画化されるが、p62顆粒などは液―液相分離によって区切られることで周囲の細胞質から区画化される。
*5 セルソーター: 特定の細胞や細胞内成分を分取する実験装置。細い管の中を通る細胞懸濁液や細胞破砕液にレーザーを照射し、蛍光や散乱光を測定することで細胞や細胞小器官を分別する。
*6 ヴォルト(vault): 1986年に発見された機能未知の巨大なたんぱく質複合体であり、細胞小器官の一種。形がアーチ型天井に似ていることからヴォルトと名付けられた。リボソームの約3倍のサイズを有する。内部は空洞であるが、ノンコーディングRNAやいくつかのたんぱく質も存在する。ほとんどの組織の細胞に存在し、1細胞あたり1000コピー以上存在する。
*7 非アルコール性脂肪性肝炎(NASH: nonalcoholic steatohepatitis): アルコール多飲を原因としない脂肪肝から進行する肝臓病。メタボリックシンドロームの増加に伴って近年増加している。
*8 マロリー・デンク体: 肝細胞がんなど肝疾患において、肝細胞内に出現するp62やユビキチン化たんぱく質陽性の構造体。構成成分や病態との関連はほとんど不明。
研究者のコメント
本研究により、これまで全く知られていなかったオートファジー経路「ヴォルトファジー」の存在が初めて明らかになりました。本研究成果は、将来的に肝細胞がんや神経変性疾患等のオートファジー関連疾患の病態解明や治療法開発につながる可能性があります。
なお本研究の共同第一著者である来栖玲央(医学部5年生)、藤本侑生(医学部6年生)は順天堂大学の基礎研究医養成プログラムに属する医学部生であり、医学部2年生から医学部のカリキュラムに加えて基礎研究に取り組み、今回論文出版に至りました。順天堂大学は基礎研究を志望する学生に早期から支援し、将来の医学界を牽引する人材を育成することを目標に今後も教育プログラムの整備を進めていきます。
原著論文
本研究はDevelopmental Cell誌のオンライン版に2023年5月15日付で公開されました。
英文タイトル: Integrated proteomics identifies p62-dependent selective autophagy of the supramolecular vault complex
タイトル(日本語訳):統合的プロテオミクス解析を用いた、超分子複合体vaultのp62依存的選択的オートファジーの発見
著者:Reo Kurusu1,#, Yuki Fujimoto1,#, Hideaki Morishita1,#,*, Daisuke Noshiro2, Shuhei Takada1, Koji Yamano3, Hideaki Tanaka4, Ritsuko Arai5, Shun Kageyama1, Tomoko Funakoshi1, Satoko Komatsu-Hirota1, Hikari Taka6, Saiko Kazuno6, Yoshiki Miura6, Masato Koike7, Toshifumi Wakai8, Satoshi Waguri5, Nobuo N Noda2, Masaaki Komatsu1,#,*
#:co-first authors
*:co-corresponding authors
著者(日本語表記):来栖玲央1,#、藤本侑生1,#、森下英晃1,#,*、能代大輔2、高田周平1、山野晃史3、田中秀明4、荒井律子5、蔭山俊1、船越智子1、小松(廣田)聡子1、高ひかり6、數野彩子6、三浦芳樹6、小池正人7、若井俊文8、和栗聡5、野田展生2、小松雅明1,*
#:共同筆頭著者
*:共同責任著者
著者所属:1)順天堂大学器官・細胞生理学分野、2)北海道大学遺伝子病制御研究所、3)東京医科歯科大学 難治疾患研究所 難治病態研究部門、4)大阪大学蛋白質研究所、5)福島県立医科大学医学部解剖・組織学講座、6)順天堂大学研究基盤センター生体分子研究室、7)順天堂大学神経生物学・形態学講座、8)新潟大学消化器外科
DOI: 10.1016/j.devcel.2023.04.015
本研究はJSPS科研費(19H05706, 21H004771, 20H03213, 23H02441)、AMED-PRIME「選択的オートファジーによるin vivoでのプロテオスタシス制御とその破綻による病態の理解」(21gm6410019h0001)、AMED-CREST(22gm1410004s0103)、武田科学振興財団、三菱財団、稲盛財団、岸本基金などの支援を受け実施されました。なお、本研究にご協力いただいた皆様には深謝いたします。
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
