iPS細胞を用いた人工血小板の作製の効率化に成功
血小板のテイラーメイド医療に向けた一歩
千葉大学大学院医学研究院の高山直也 准教授、江藤浩之 教授、北海道大学の曽根正光 助教(2019年12月まで千葉大学特任助教)、京都大学iPS細胞研究所の中村壮 特任助教らの研究チームは、ヒトiPS細胞(注1)から血小板を産生するための従来法よりも効率的な手法の開発に取り組みました。その結果、細胞の増殖を妨げるCDKN1Aとp53という2つの遺伝子の働きを抑えることで、高効率に血小板産生細胞を得られることが分かりました。
この結果により、従来の血小板輸血では治療が困難な血小板不応症(注2)の患者さんの治療にもつながることが期待されます。
本研究成果は、2021年12月2日に、学術誌Stem Cell Reportsでオンライン公開されました。
この結果により、従来の血小板輸血では治療が困難な血小板不応症(注2)の患者さんの治療にもつながることが期待されます。
本研究成果は、2021年12月2日に、学術誌Stem Cell Reportsでオンライン公開されました。
- 研究の背景
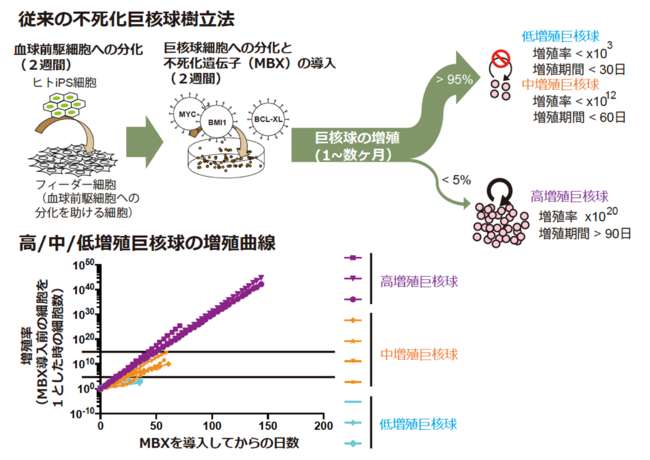 図1:従来の不死化巨核球樹立法と得られた巨核球の増殖曲線
図1:従来の不死化巨核球樹立法と得られた巨核球の増殖曲線
しかし、多能性幹細胞から不死化巨核球を樹立できる確率は5%以下と低く、ほとんどの試行においてMBXを発現させても巨核球が増殖を2ヶ月以内に停止してしまうという問題がありました(図1上)。また増殖能力の低い巨核球は、一つの巨核球あたりから産生される血小板数も低いということが分かっていました。そこで研究チームは巨核球が不死化する確率が高くなるよう手法の改善を目指しました。
- 研究の成果
その結果、CDKN1A遺伝子に対するshRNAを導入した場合と、CDKN1Aの発現を促進するp53遺伝子に対するshRNAを導入した場合に、最終的に100倍以上の細胞数が得られ、増殖が著しく改善されました(図2左)。一方、CDKN2Aに対するshRNAにはそのような増殖促進効果はありませんでした。
次に、研究チームは新たにiPS細胞から巨核球を分化する過程でこれらのshRNAを導入し、巨核球の不死化効率が改善するかどうかを調べました(図2右)。その結果、MBXに加えてCDKN1Aとp53に対するshRNAを同時に導入することで、増殖期間が4倍程度、増殖率が10の10乗以上と増殖能力が飛躍的に改善しました。
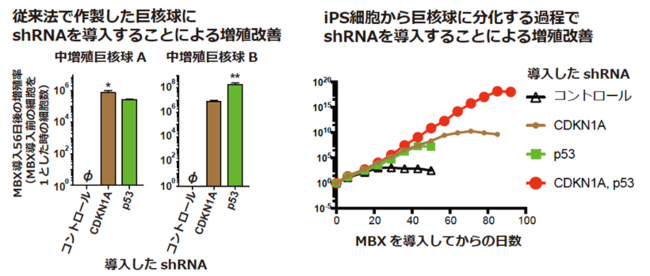 図2:CDKN1A, p53に対するshRNAによる巨核球の増殖改善
図2:CDKN1A, p53に対するshRNAによる巨核球の増殖改善
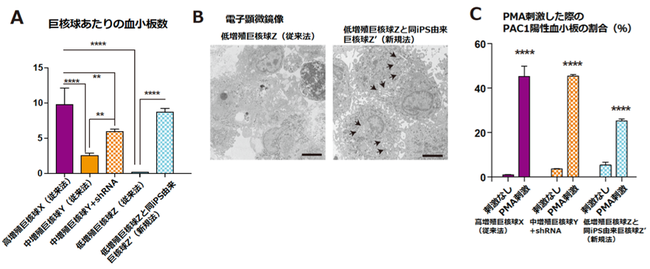 図3:shRNA導入巨核球の血小板産生能力と血小板機能の解析
図3:shRNA導入巨核球の血小板産生能力と血小板機能の解析
- 今後の展望
- 用語解説
(注2)血小板不応症:血小板輸血を繰り返すことで、体内で輸血血小板に対する抗体が産生され、輸血血小板が速やかに排除されてしまう症状。この状態に陥ると血小板輸血が無効化され、治療が困難となる。
(注3)多能性幹細胞:初期胚と同様に様々な細胞に分化する能力を持つ幹細胞で、前述のiPS細胞と胚性幹細胞(ES細胞)を含む。
(注4)不死化:一般的に細胞が分裂できる回数は有限であるが、増殖を促進するタンパク質を発現させることなどにより、その制限を超えて無限に増殖できる状態にすること。
(注5)RNA-seq法:近年開発された次世代シーケンサーと呼ばれる装置を用いて、細胞や組織における遺伝子の発現状態を網羅的に解析する手法。
(注6)shRNA:short hairpin RNAの略。細胞に導入することで標的とする遺伝子のメッセンジャーRNAを破壊し、その遺伝子の機能を抑制することができる。
(注7)DMS:demarcation membrane systemの略。血小板産生が旺盛な巨核球に見られる特殊な細胞内膜構造。
(注8)PMA刺激:Phorbol 12-myristate 13-acetateの略。血小板内のプロテインキナーゼCという酵素を活性化することで、血小板の活性化を引き起こす。
(注9)PAC1:血小板がかさぶた (血栓) を作る際にインテグリンという分子が活性化し、周囲の血小板同士が架橋され、血栓として強固となっていく。PAC1抗体は活性型のインテグリン分子に特異的に結合する抗体。
- 論文情報
著者:Masamitsu Sone, Sou Nakamura, Sachiko Umeda, Harumi Ginya, Motohiko Oshima, Maria Alejandra Kanashiro, Sudip Kumar Paul, Kanae Hashimoto, Emiri Nakamura, Yasuo Harada, Kyoko Tsujimura, Atsunori Saraya, Tomoyuki Yamaguchi, Naoshi Sugimoto, Akira Sawaguchi, Atsushi Iwama, Koji Eto, and Naoya Takayama
雑誌名:Stem Cell Reports
DOI:https://doi.org/10.1016/j.stemcr.2021.11.001
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザーログイン既に登録済みの方はこちら
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
