白血病を含むがんの新規創薬へ前進
―エピゲノム酵素がミトコンドリアの呼吸制御に関わるメカニズムを解明―
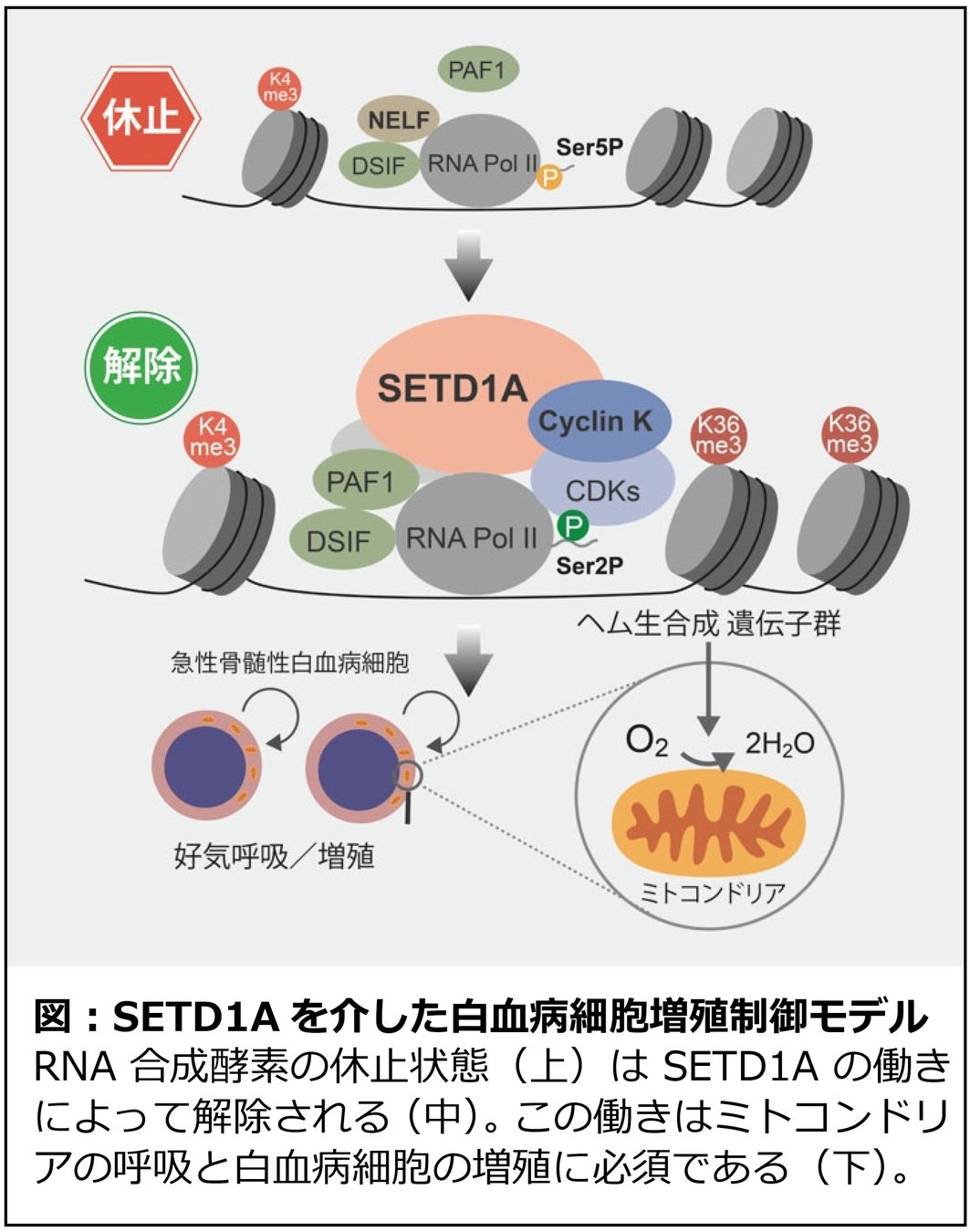
千葉大学大学院医学研究院の星居孝之講師、医学部医学科5年の菊地創太、大学院医学研究院の金田篤志教授らの研究チームは、蛋白質の分解を誘導する技術を駆使し、急性骨髄性白血病細胞の核内にあるヒストンメチル化酵素であるSETD1A(注1)を分解すると、白血病細胞が死滅することを確認しました。またさらに詳しい解析により、SETD1Aがミトコンドリアの呼吸を制御するメカニズムを明らかにしました(下図)。
本研究成果は、科学誌「Cell Reports」にて2022年11月30日(日本時間)にオンライン公開されました。
本研究成果は、科学誌「Cell Reports」にて2022年11月30日(日本時間)にオンライン公開されました。
- 本研究成果のポイント
② 本研究では、SETD1Aというヒストンメチル化酵素が、遺伝子発現を介したミトコンドリアの機能制御によって、より直接的にがん細胞の増殖や生存に関わることを明らかにしました。
③ 今後は、SETD1Aの異常を示す疾患や白血病やがんなど、ミトコンドリア異常と関連が深い疾患の新たな治療法の確立につながることが期待されます。
- 研究の背景
本研究にて国際共同研究を行なったNabet博士らのグループ(フレッドハッチンソンがん研究センター、アメリカ)では、低分子化合物にて蛋白分解を誘導するdTAGシステムが開発されています。通常の薬では酵素活性を持たないタンパク質を標的とすることは困難とされてきましたが、dTAGシステムを含む標的タンパク質分解誘導薬化合物(PROTAC)(注2)では薬剤の標的となるタンパク質自体が分解されるため、酵素活性に依存しない機能を阻害することが可能です。
- 研究の成果
1) SETD1Aはミトコンドリアのヘム生合成(注3)に関わる遺伝子の発現を制御する
2) 白血病細胞はヘム生合成関連遺伝子を必要とする
3) SETD1Aは転写の休止解除(注4)に必要である
4) SETD1A-Cyclin K経路が転写休止解除とミトコンドリアの呼吸制御に関わる
今回の研究により、ヒストンメチル化酵素SETD1Aが転写の休止解除の制御を介してミトコンドリアの機能制御を行うことが明らかとなりました。SETD1Aは統合失調症の関連遺伝子として報告されておりますが、その仕組みはまだ良く分かっていません。ミトコンドリアの機能異常はがんだけでなく、精神疾患の要因としても考えられており、SETD1Aの活性化や機能異常がもたらす細胞内代謝の異常は、新たな創薬の標的となることが考えられます。
- 研究者のコメント(千葉大学大学院医学研究院 星居講師)
- 用語解説
(注2)標的タンパク質分解誘導薬化合物(PROTAC): 標的とすべきタンパク質への結合性を有する分子と、タンパク質分解酵素であるユビキチン E3 リガーゼへの結合性を有する低分子を適切な長さのリンカーで連結した、標的タンパク質の分解を誘導する低〜中分子化合物の一種。
(注3)ヘム生合成:細胞質とミトコンドリアで起こる一連の酵素反応で、最終産物としてヘムを生成する。
(注4)転写休止解除:RNA合成酵素は転写に必要なタンパク質複合体を形成した後に、転写開始点近傍にて休止状態をとる。上流からの刺激によって休止が解除されると、その後の転写反応が進行する。遺伝子発現のチェックポイントとして働き、発現量の調整や同調的な遺伝子の発現に関与している。
- 論文情報
・著者:Takayuki Hoshii, Sarah Perlee, Sota Kikuchi, Bahityar Rahmutulla, Masaki Fukuyo, Takeshi Masuda, Sumio Ohtsuki, Tomoyoshi Soga, Behnam Nabet, Atsushi Kaneda.
・雑誌名:Cell Reports
・DOI:https://doi.org/10.1016/j.celrep.2022.111727
- 研究プロジェクトについて
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザーログイン既に登録済みの方はこちら
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
