「AmoyDx®肺癌マルチ遺伝子PCRパネル」のEGFR遺伝子変異陽性非小細胞肺癌に対するアミバンタマブとラゼルチニブ併用療法適応追加の一部変更申請に関するお知らせ
― EGFR遺伝子変異陽性の切除不能な進行・再発の非小細胞肺癌に対するアミバンタマブとラゼルチニブ併用療法の適応追加の一部変更申請 ―

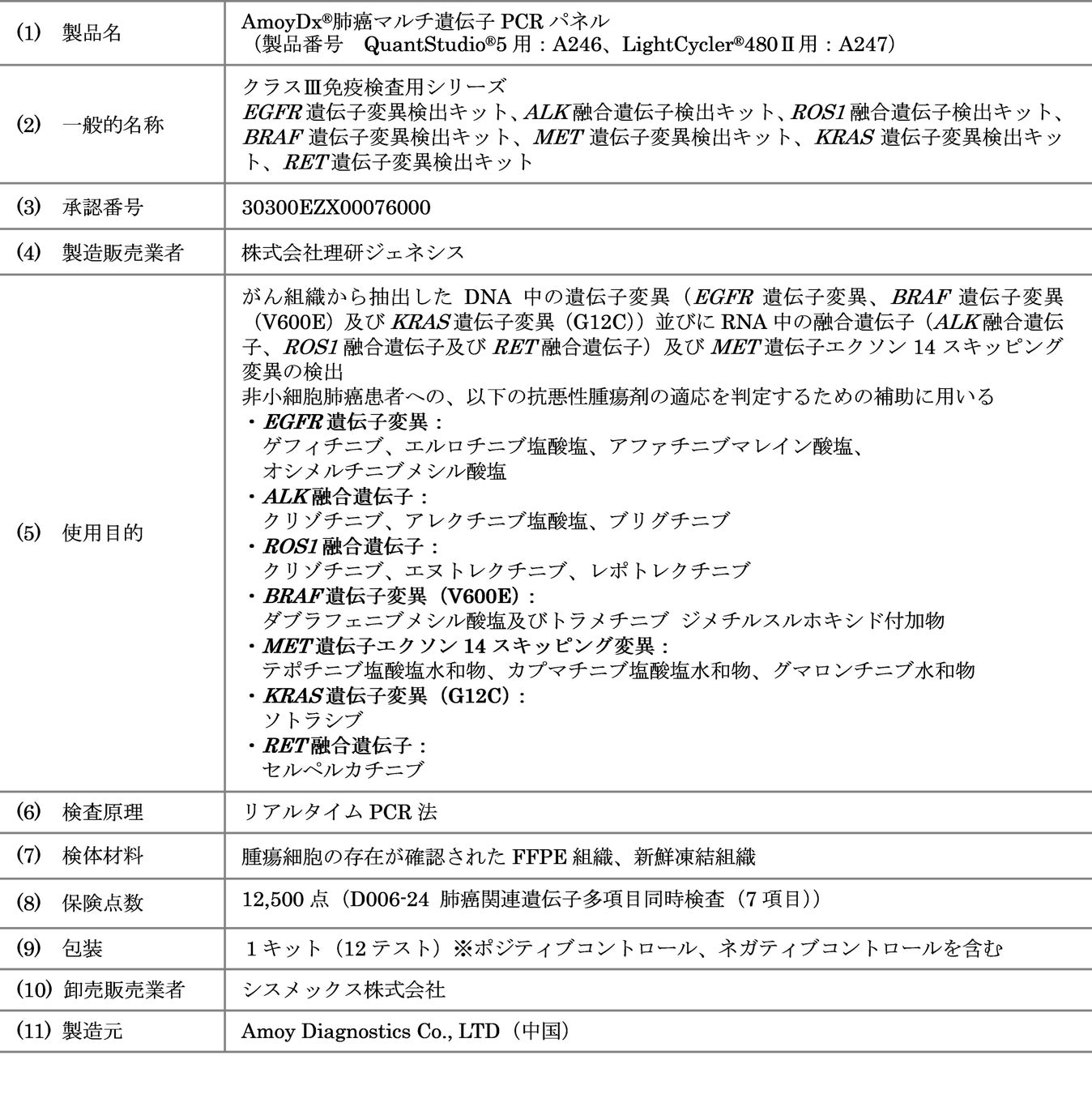
株式会社理研ジェネシス(本社:東京都品川区、代表取締役社長:岩壁賢治)は、EGFR遺伝子変異(エクソン19欠失変異、エクソン21 L858 R変異を含む)陽性の切除不能な進行・再発の非小細胞肺癌に対して、上皮成長因子受容体(EGFR)及び間葉上皮転換因子(MET)を標的とする二重特異性抗体である「ライブリバント®点滴静注350mg」(一般名:アミバンタマブ[遺伝子組換え]、製造販売元:Johnson & Johnson (法人名:ヤンセンファーマ株式会社、本社:東京都千代田区)と、経口第3世代EGFRチロシンキナーゼ阻害薬(EGFR-TKI)であるラゼルチニブの併用療法の追加適応を取得するために、体外診断用医薬品「AmoyDx®肺癌マルチ遺伝子PCRパネル」(以下「本製品」)の製造販売承認事項一部変更申請を厚生労働省に行いましたことをお知らせいたします。
今後、アミバンタマブとラゼルチニブ併用療法に対する追加適応の承認が得られることで、EGFR遺伝子陽性の切除不能又な進行・再発の非小細胞肺癌患者に対して、同併用療法のコンパニオン診断薬として本製品の使用が可能となり、治療機会の拡大に貢献することが期待されます。
本製品は、非小細胞肺癌の7種のドライバー遺伝子(EGFR、ALK、ROS1、BRAF、MET、KRAS、RET )をカバーする、リアルタイムPCR法を原理とした体外診断用医薬品です。
7種のドライバー遺伝子のマルチプレックス検査として、EGFR遺伝子変異、ALK融合遺伝子、ROS1融合遺伝子、BRAF遺伝子変異(V600E)、MET遺伝子エクソン14スキッピング変異、KRAS 遺伝子変異(G12C)、RET融合遺伝子を一回の測定で同時に検査が可能であり、現在16種の抗悪性腫瘍剤の適応判定の補助として承認されています。
株式会社理研ジェネシスについて:
理研ジェネシスは、最先端の遺伝⼦解析技術やバイオインフォマティクスを活⽤した遺伝⼦受託解析サービスや製品を提供し、個別化医療における技術・経験・ノウハウを保有する数少ない⽇本企業の⼀つです。2007年、凸版印刷株式会社(以下「凸版印刷」、現TOPPANホールディングス株式会社)、国⽴研究開発法⼈理化学研究所(以下「理化学研究所」)および株式会社理研ベンチャーキャピタルの共同で、個別化医療における理化学研究所の最先端研究成果を広く社会に展開し医療現場における実⽤化を促進することを⽬指し設⽴されました。2014年、凸版印刷およびシスメックス株式会社(以下「シスメックス」)が、個別化医療における遺伝⼦検査事業の発展のため、相互に協⼒していくことに合意し、それぞれ理研ジェネシスに出資。さらに 2016 年、ゲノム医療の臨床実装の実現に向けて、シスメックスの⼦会社となりました。詳しくは、以下のウェブサイト(https://www.rikengenesis.jp/)をご覧ください。
本件に関するお問合せ先:
株式会社理研ジェネシス マーケティング部
Eメール:info2@rikengenesis.jp
電話番号:03-5759-6042
すべての画像
