広範なアジドを合成する新たな方法を確立
~医薬品として有用な1,2,3-トリアゾール類の合成が容易に~
【研究の要旨とポイント】
保護されたアジド基を有するGrignard反応剤を用いたアジド化合物の合成法の確立に成功しました。
本手法により合成されたアジド化合物を原料としたクリック反応により、1,2,3-トリアゾール類を合成することに成功しました。
本研究をさらに発展させることで、多種多様なアジド化合物、1,2,3-トリアゾール類を容易に得ることができ、医薬品開発などへの貢献が期待されます。
【研究の概要】
東京理科大学先進工学部生命システム工学科の吉田優准教授、浪岡璃奈氏(2023年度修士課程2年)、鈴木美之里氏(2021年度特別研究生、2021年度東京医科歯科大学修士課程修了)の研究グループは、保護されたアジド基を有するGrignard反応剤の調製法を発見し、広範なアジド化合物を合成する新しい手法の確立に成功しました。また、本手法により得られたアジド化合物を原料として使用することで、さまざまな置換基を有する1,2,3-トリアゾール類を合成できることを実証しました。
アジド化合物は有機合成、薬学、材料科学などさまざまな分野で利用される重要な化合物です。特に、アジドとアルキンによる環化付加反応はクリック反応として知られており、複雑な合成法を用いることなく、分子同士を容易に結合することができます。一方で、アジド基は高い反応性を有するため、反応における制約が多く、合成できる化合物が限定されてしまうことが課題でした。これに対して、本研究グループは、著者らが以前開発した「アジド基保護法」によりアジド基の反応性を抑制した状態のGrignard反応剤を得ることができれば、この課題を解決できるのではないかと着想し、研究に取り組んできました。
本研究では、ヨウ化アリール中のアジド基を有機リン化合物Amphos([4-(N, N-ジメチルアミノ)フェニル]ジ-tert-ブチルホスフィン)で保護してアジド基の反応性を抑制した後でも、ターボGrignard試薬(イソプロピルマグネシウムクロリド-塩化リチウム錯体)を反応させると、ヨウ素-マグネシウム交換反応が進行することを明らかにしました。そして、生じた有機マグネシウム中間体によるGrignard反応で、マグネシウム部分(ヨウ化アリールのヨウ素部分)が他の置換基に変化したアジド化合物を合成することに成功しました。この手法で合成したアジド化合物とアルキンのクリック反応により、1,2,3-トリアゾール類を合成できることを実証しました。
本手法を応用すると、さまざまな置換基を有するアジド化合物や1,2,3-トリアゾール類を容易に合成できるようになるので、創薬や有機合成に大きく貢献することが期待されます。
本研究成果は、2023年7月31日に国際学術誌「Frontiers in Chemistry」にオンライン掲載されました。
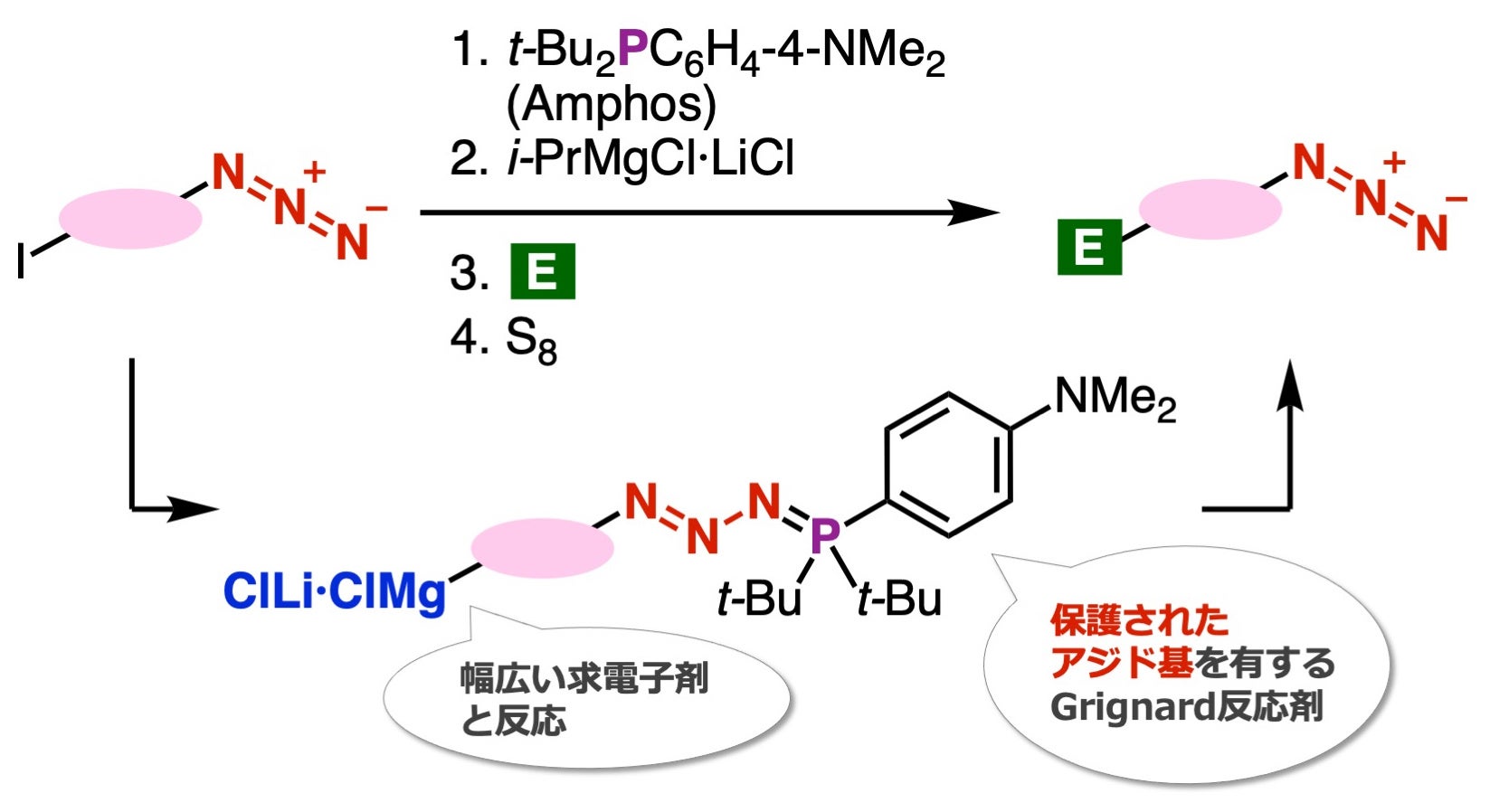
図 本研究における主要な反応
【研究の背景】
クリック反応とは、2つの異なる分子をブロックでカチッとくっつけたように、きれいに素早く進行する反応のことを指します。適用範囲が広い、操作や精製が簡便、副生成物が少なく目的物を高収率で得られるなどの優れた特徴を有しています。複雑な分子同士を容易に結合させて付加価値の高い化合物を合成できることから、有機合成における工程の短縮化や時間削減への貢献が期待されています。代表的なクリック反応として、アジドとアルキンにより1,2,3-トリアゾール類を合成する環化付加反応が挙げられます。例えば、銅触媒を用いたアジド-アルキン環化付加(CuAAC: Cu(I)-catalyzed azide-alkyne cycloaddition)や歪み促進型アジド-アルキン環化付加(SPAAC: strain-promoted azide-alkyne cycloaddition)が広く知られています。一方で、クリック反応に欠かせないアジド化合物は求電子的な性質を持ち、反応性が高いため、合成における制約が多く、広範な化合物を得られないことが課題となっていました。
本研究グループは過去の研究で、有機リン化合物であるAmphosがアジド基とスムーズに反応してホスファジドを生成すること、また生成したホスファジドを硫黄で脱保護することで元のアジド基に変換できることを見出していました。これらの知見から、吉田准教授らは、ヨウ化アリールのアジド基をAmphosで保護した後、ターボGrignard試薬と反応させることで、保護されたアジド基を有するGrignard反応剤を得られるのではないかという考えに至りました。これにより、アジド部分の反応性を抑えた状態でのGrignard反応が可能となり、分子内に他の置換基を導入できると期待されます。今回、本研究グループは、Grignard反応によりヨウ化アリールのヨウ素部分にさまざまな置換基を導入し、多種多様なアジド化合物とそれを原料とした1,2,3-トリアゾールの合成を行いました。
【研究結果の詳細】
① アジド化合物の合成
はじめに、アジド基を有するヨウ化アリールにおいて、ヨウ素-マグネシウム交換反応が進行するかの確認を行いました。4-アジド-4’-ヨード-1,1’-ビフェニルにAmphosを反応させてアジド基の保護を行った後、テトラヒドロフラン(THF)を溶媒として-20℃でターボGrignard試薬を加えました。反応溶液にN, N-ジメチルホルムアミド(DMF)を添加して反応をさらに進めると、ホルミル化が効率的に進行することがわかりました。最後に、硫黄を加えてアジド基を脱保護することにより、目的の4-(4-アジドフェニル)ベンズアルデヒドが収率87%で得られました。一方で、Amphosでアジド基を保護しない条件ではアジド基が分解してしまい、目的物は全く得られないことがわかりました。
次に、上記方法と同様にして調製したGrignard反応剤にさまざまな求電子試薬を加えたときに、アジド化合物の合成反応が進行するかを確認しました。その結果、ヒドロキシ基、ホルミル基、メトキシ基、チエニル基など各置換基を有するアジド化合物を高収率で合成できることがわかりました。以上の結果から、アジド基の保護を行ったヨウ化アリールのGrignard反応により、幅広いアジド化合物を合成できることが実証されました。
② 1,2,3-トリアゾール化合物の合成
合成したアジド化合物とアルキンのクリック反応により、さまざまな1,2,3-トリアゾール類の合成を行いました。①の手法と同様に、ヨウ化アリールにAmphosを加えて調製した後、ターボGrignard試薬を加えて、保護されたアジド基を有するGrignard反応剤を得ました。アルデヒドとGrignard反応により新たなアジド化合物を合成した後、硫黄でアジド基の脱保護を行いました。その後、アルキンとのCuAACを行うことで、対応する1,2,3-トリアゾールを合成できることを確認しました。
本研究を主導した吉田准教授は「アジド基は反応性が高いので、その分アジド化合物を合成するときの制約が大きくなります。しかし、私たちが発見したアジド基保護法を利用すれば、幅広いアジド化合物を簡便に合成することができます。アジド化合物はクリックケミストリーにおいて中心的な役割を担いますので、医薬品等の効率的な開発への貢献が期待されます」と、研究の意義を語っています。
※本研究は、日本学術振興会の科研費(JP22H02086)、旭硝子財団の助成を受けて実施されました。
【論文情報】
雑誌名:Frontiers in Chemistry
論文タイトル:Synthesis of 1,2,3-triazoles using Grignard reactions through the protection of azides
著者:Rina Namioka, Minori Suzuki, and Suguru Yoshida
DOI:10.3389/fchem.2023.1237878
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
