チオエステルの直接酸化によりスルフィン酸エステルを簡便に合成
~創薬や材料化学に有用な有機硫黄化合物の調製が容易に~
【研究の要旨とポイント】
チオエステルを直接酸化することにより、スルフィン酸エステルを簡便に合成する手法を開発しました。
入手しやすいヨウ化アリールを原料として、わずか2工程でスルフィン酸エステルを合成できます。
本研究をさらに発展させることで、さまざまな有機硫黄化合物の調製が容易となり、医薬品や有機合成分野への貢献が期待されます。
【研究の概要】
東京理科大学先進工学部生命システム工学科の吉田優准教授、中村圭佑氏(2023年度 修士課程1年)、熊谷幸子氏(2023年度 修士課程1年)、鈴木美之里氏(2021年度 特別研究生、2021年度 東京医科歯科大学 修士課程修了)、小林瑛宏氏(2021~2023年度 特別研究生、2023年度 東京医科歯科大学 博士課程3年)の研究グループは、チオエステルを直接酸化することによりスルフィン酸エステルを効率よく合成する手法の開発に成功しました。また、ヨウ化アリールを出発原料として、スルフィン酸エステルを2つの工程で得る手法を確立しました。
スルフィン酸エステルなどの有機硫黄化合物は、医薬品開発の基質や有機合成材料として欠かせない重要な物質です。従来、これらの合成にはチオールを直接酸化する方法が用いられてきました。しかしながら、原料のチオールは、その悪臭や、空気中での安定性の低さなどのため扱いにくく、多くの課題がありました。また、チオールをエステル化して得られるチオエステルの酸化反応も検討されてきましたが、硫黄原子に電子求引性のカルボニル基が結合しているため酸化反応が進行しにくいことから、チオエステルの直接酸化によるスルフィン酸エステル合成は困難とされてきました。
これに対して、本研究グループは、チオエステルの直接酸化によるスルフィン酸エステルの合成法の確立を目指して、反応経路の開拓や反応条件の検討を行ってきました。
本研究での検討の結果、ヨウ化アリールを出発原料としてわずか2つの工程で目的のスルフィン酸エステルを合成することに成功しました。第1の工程では、ヨウ化銅(I)CuI触媒を用いたC−S結合形成反応によって、チオエステル化合物を合成します。第2の工程では、得られたチオエステル化合物をN-ブロモスクシンイミド(NBS)などの反応剤を利用して直接酸化し、目的のスルフィン酸エステルを合成します。
出発原料であるヨウ化アリール類は容易に入手できるため、今回確立した合成法は汎用性の高い手法といえます。また、生成物であるスルフィン酸エステルはさまざまな有機合成に利用可能であることから、幅広い分野での応用が期待されます。
本研究成果は、2023年8月11日に国際学術誌「Organic & Biomolecular Chemistry」にオンライン掲載されました。
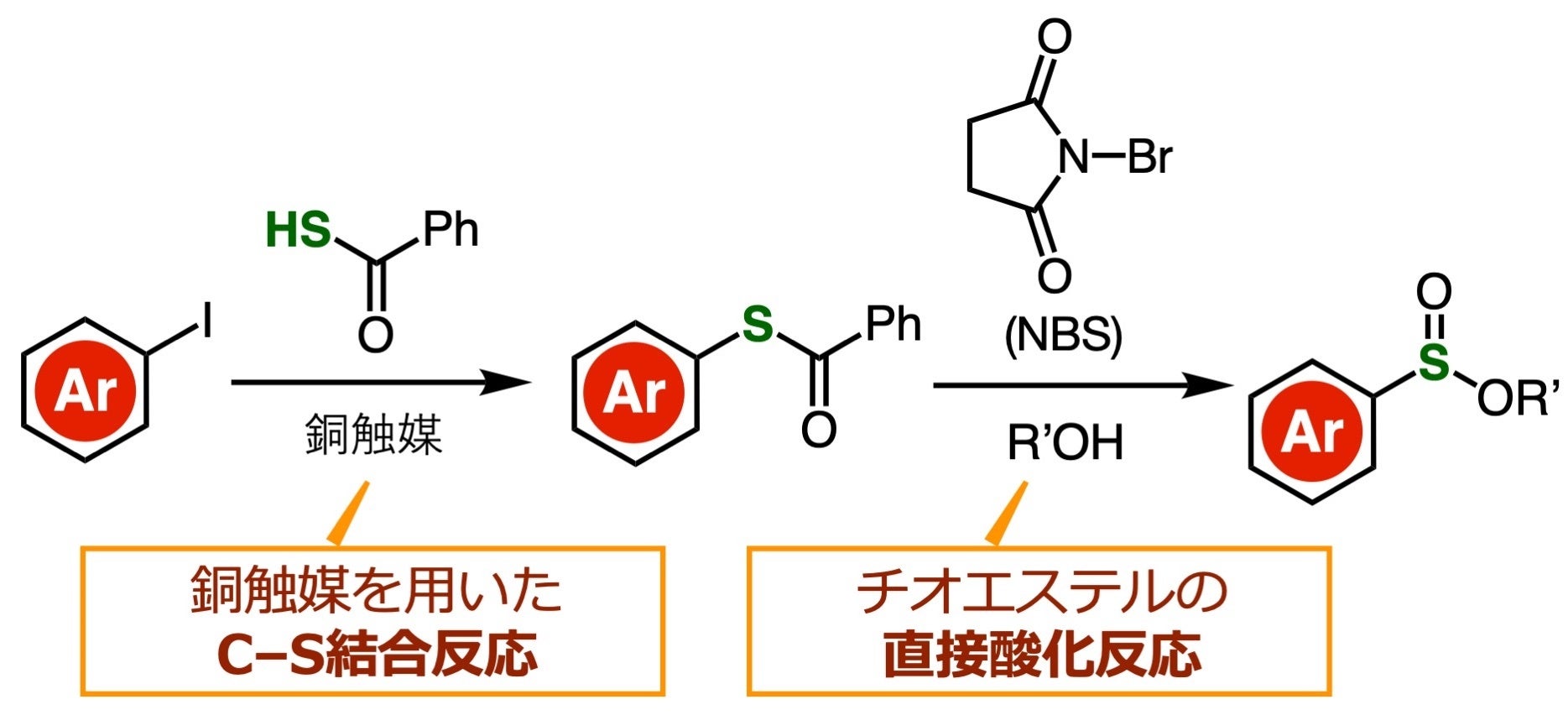
図 本研究における主要な反応
【研究の背景】
チオエステルは、電子求引性を有するカルボニル基により、硫黄原子の求核性や酸化性が低下することから、有機硫黄化合物を調製する際のチオールの保護体として使用されてきました。スルフィン酸エステルを合成するために、チオエステルを直接酸化する方法が検討されてきましたが、上述の理由により酸化反応が起こりにくいことに加え、過剰酸化によるスルフィン酸エステルの分解の可能性もあるため、実現が難しいと考えられてきました。
本研究グループは過去に、スルフィン酸エステルを変換し、高機能化スルホキシドやスルフィドの合成に成功したことを報告しています。今回はこれらの知見を活かし、チオエステルの直接酸化によるスルフィン酸エステルの効率的な合成法の開発に着手しました。
【研究結果の詳細】
① チオエステルの直接酸化
まず、チオエステルの直接酸化反応に関する条件検討を行いました。その結果、チオエステルにN-ブロモスクシンイミド(NBS)を添加して反応させると、スルフィン酸エステルを効率よく得られることを見出しました。一方で、NBSの代わりにN-クロロスクシンイミド(NCS)やN-ヨードスクシンイミド(NIS)を用いると、望みの反応はほとんど進行しないことがわかりました。また、反応時間を長くすると過剰酸化により収率が著しく低下することも明らかとなりました。これらの結果から、NBSを臭素化剤とする酸化反応により、チオエステルからスルフィン酸エステルを効率よく合成できることが実証されました。
② ヨウ化アリールを出発原料としたワンポット合成
CuI触媒を用いてヨウ化アリールとチオ安息香酸のC−S形成を行った後、NBSで酸化することによりスルフィン酸エステルをワンポットで合成することに成功しました。本手法では、メチル基、フルオロ基、ブロモ基、トリフルオロメチル基、メトキシカルボニル基などさまざまな置換基を有するチオエステルを効率的にスルフィン酸エステルに酸化することが可能です。また、残ったチオ安息香酸を塩基性水溶液で簡単に除去できるため、悪臭を伴うことなくスルフィン酸エステルを合成できる点も特筆に値します。
③ チオエステル酸化反応機構の解明
本研究ではチオエステルの酸化反応の機構解明も行いました。提案した反応機構は以下の通りです。
(a): 最初にNBSによりチオエステルが直接酸化される。
(b): 生成した中間体とメタノールが反応し、安息香酸メチルを副生しながら、スルフェニル臭化物が生成される。
(c): 生成したスルフェニル臭化物とメタノールの反応によって、スルフェニルエステルを生成する。
(d): スルフェニルエステルの酸化が進行し、さらにメタノールとのエステル交換反応が生じ、目的のスルフィン酸エステルが得られる。
本研究を主導した吉田准教授は「一般的に、チオエステルがカルボニル基と結合するとアシル基が保護基としてはたらくため、酸化反応が進行しにくくなると予想されます。しかしながら私たちは、硫黄原子の特性を利用した直接酸化の条件を見出すことができると確信していました。今回合成したスルフィン酸エステル類は広範な有機硫黄化合物の合成に有用です。そのため、医薬品をはじめとしたさまざまな機能を有する有機硫黄化合物の開発に資すると考えています」と、研究の意義を語っています。
※本研究は、日本学術振興会の科研費(JP22H02086)、上原記念生命科学財団、徳山科学技術振興財団、UBE学術振興財団、稲盛財団の助成を受けて実施されました。
【論文情報】
雑誌名:Organic & Biomolecular Chemistry
論文タイトル:Facile synthesis of sulfinate esters from aryl iodides via direct oxidation of thioesters
著者:Keisuke Nakamura, Yukiko Kumagai, Akihiro Kobayashi, Minori Suzuki and Suguru Yoshida
DOI:10.1039/d3ob01108a
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
