破骨細胞の分化に関わる必須因子を発見
~mRNAスプライシングの制御が鍵、骨粗鬆症治療薬開発の基盤となる成果~
【研究の要旨とポイント】
破骨細胞の過剰な活性化は骨粗鬆症や関節リウマチなどの疾患につながることから、破骨細胞分化を制御するメカニズムの解明は急務となっています。
今回、RNA結合タンパク質『細胞質ポリアデニル化エレメント結合タンパク質4(Cpeb4)』が、RNAに結合する機能を介して核内構造体に局在し、破骨細胞の分化に関わる転写因子のmRNAスプライシングを部分的に制御していることが示唆されました。
本研究は、破骨細胞分化を制御するメカニズムの一端を明らかにしたものであり、骨粗鬆症や関節リウマチの病態解明や新たな治療薬開発の基盤となる重要な成果です。
【研究の概要】
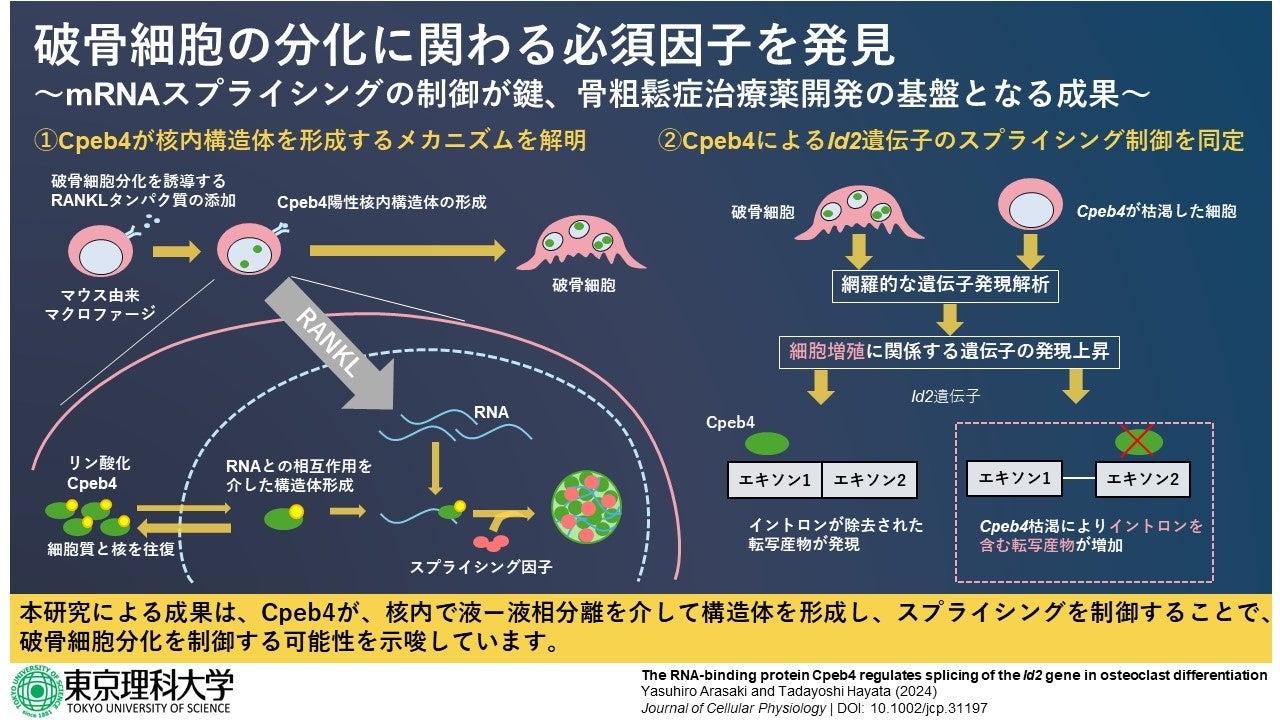
東京理科大学 薬学部生命創薬科学科の早田 匡芳教授と同大学 薬学研究科薬科学専攻の荒崎 恭弘氏(2023年度博士後期課程3年)は、RNA結合タンパク質の1種である『細胞質ポリアデニル化エレメント結合タンパク質4(Cpeb4)』が、mRNAのスプライシング(*1)制御を介して、破骨細胞の分化に重要な役割を果たしていることを明らかにしました。
本研究グループはこれまでに、Cpeb4は破骨細胞の分化に伴い、核内構造体に局在することが明らかにしていましたが(※1)、局在のメカニズムや機能は不明でした。核内構造体ではmRNAの成熟化に関わるスプライシングが行われていますが、今回、Cpeb4は、RNAに結合する機能を介して、核内構造体に局在することがわかりました。さらに、Cpeb4欠損細胞では、破骨細胞の分化に関わる転写因子のmRNAのスプライシングパターンが変化しました。これらの結果は、Cpeb4が、mRNAのスプライシングを介して、破骨細胞の分化を制御していることを示す結果です。
破骨細胞は、骨粗鬆症などの骨疾患の治療標的として盛んに研究が進められている細胞です。本研究ではマウスの培養細胞を用いましたが、ヒトにおいても、CPEB4遺伝子多型と骨密度が相関しているという研究報告もあります。本成果は、骨粗鬆症や関節リウマチの病態解明や新たな治療薬開発の基盤となる重要な知見となります。
本研究成果は、2024年1月29日に国際学術誌「Journal of Cellular Physiology」にオンライン掲載されました。
※1 過去のプレスリリース
『破骨細胞への分化を促進するRNA結合タンパク質を同定 ~骨や関節の疾患における病態解明や治療薬開発につながる可能性~』
URL: https://www.tus.ac.jp/today/archive/20200609_1020_1.html
【研究の背景】
高齢化が進む日本では骨粗鬆症患者は増加傾向にあり、現在1300万人以上が罹患していると推定されています。骨粗鬆症の高齢者が転倒して骨折し、寝たきりになるケースも多く、社会問題となっています。既存の治療法では十分な効果が得られない患者も多いことから、新たな治療薬の開発が待たれています。
骨粗鬆症は、閉経や加齢により、骨代謝のバランスが崩れ、骨が脆くなった状態です。破骨細胞は古くなった骨を吸収する細胞で、新しい骨を形成する骨芽細胞とともに骨の新陳代謝を担っています。破骨細胞の過剰な活性化は、骨粗鬆症や関節リウマチなどの骨疾患における骨減少や骨破壊の原因となることから、破骨細胞は骨粗鬆症をはじめとする骨疾患の治療標的となっています。
破骨細胞は骨髄造血幹細胞由来の単球・マクロファージ系前駆細胞から分化して形成されます。前駆細胞から破骨細胞への分化が亢進すると骨代謝のバランスが崩れ、骨破壊が誘導されることから、破骨細胞分化の詳細なメカニズムの解明が課題となっています。
これまで、破骨細胞の分化に関わるシグナル伝達経路や転写調節因子のはたらきについては、数多く報告され、知見の蓄積が進んでいます。一方、mRNAスプライシングなどのmRNA代謝と破骨細胞分化の関係はまだよくわかっていません。しかし近年、破骨細胞の分化と機能の制御には、mRNAのスプライシングや安定性制御、翻訳制御といった転写後の制御が不可欠であることが明らかになりつつあります。
これまでに本研究グループは、RANKL(*2)による破骨細胞分化においては、mRNAの転写後調整を行うCpeb4の存在が必須であり、核内構造体に局在することを発見・報告していました。しかし、Cpeb4の局在を引き起こすメカニズムや、核内構造体においてCpeb4が果たす役割についてはわかっていませんでした。
【研究結果の詳細】
RANKL処理を施したマウスマクロファージ様細胞株RAW264.7において、RANKL処理によってCpeb4のリン酸化レベルが上昇しているかどうかを、ポリアクリルアミド電気泳動(SDS-PAGE)(*3)で調べました。その結果、Cpeb4はRANKL処理前にすでに高度にリン酸化されており、RANKL処理9時間後も変化はなかったことから、Cpeb4の局在変化はリン酸化レベルの変化とは無関係であることが示唆されました。また、ヒト胎児腎臓由来細胞株HEK293Tにトランスフェクション(*4)したCpeb4は、RANKL処理したRAW264.7細胞と同様に核内構造体に局在したことから、HEK293T細胞においては、Cpeb4の局在にはRANKLシグナルは必要ではないということが示唆されました。さらに、Cpeb4を発現しているHEK293T細胞で、タンパク質の核外輸送を阻害すると、Cpeb4は核全体に集積しました。この結果は、Cpeb4はシグナル伝達を介さずに細胞質と核の間を往復していることを示唆します。
次に、核内構造体への局在に必要なCpeb4の領域を同定しました。RNA結合タンパク質は通常、特定の構造を持たない不安定なアミノ酸配列である天然変性タンパク質(IDR)と、RNAを認識する領域を持っています。転写や選択的スプライシングなどのRNA代謝全般に関わるFused in sarcoma(FUS)のようなRNA結合タンパク質は、液—液相分離(*5)を媒介するIDRを持ち、細胞質液滴(*6)を形成することが知られています。Cpeb4のタンパク質構造を予測したところ、Cped4もIDRを持つものの、これらのIDR領域を欠損させたCpeb4は、野生型Cpeb4と同様の核内局在を示しました。しかし、RNA結合領域を欠損させたCpeb4は、核内構造体には局在しませんでした。このことから、核内構造体へのCpeb4の局在は、Cpeb4のIDRを介したタンパク質間相互作用によるものではなく、Cpeb4とRNAとの相互作用によるものであると推測されました。
さらに、免疫蛍光染色および免疫沈降実験の結果、Cpeb4はスプライシング因子であるSRSF5とSRSF6と共局在し、相互作用していることが示唆されました。
最後に、破骨細胞分化の過程でCpeb4が破骨細胞分化関連遺伝子のスプライシングを制御しているかどうかを調べるため、RNA-seq解析を行いました。その結果、Cpeb4欠損によって破骨細胞分化に関わる転写調節因子であるId2のスプライシングのパターンが変化することが確認できました。
以上の結果は、Cpeb4が核内での液—液相分離を介してスプライシングを制御している可能性を示唆しています。研究を主導した早田教授は「破骨細胞が分化する過程は非常にダイナミックで、その背後にはどんなメカニズムが潜んでいるのだろうと純粋な好奇心を刺激されます。今回、その一端を明らかにでき、大変嬉しく思います。また、破骨細胞は、骨粗鬆症、関節リウマチやがんの骨転移による骨破壊にも関わっています。そうした骨疾患の病態解明や治療薬の開発に貢献したいという思いも、研究のモチベーションとなりました」と、本研究成果についてコメントしています。
※本研究は、日本学術振興会(JSPS)の科研費(21J22295、JP18K09053)の助成を受けて実施したものです。
【用語】
*1 スプライシング
mRNA前駆体の一部の領域を取り除き、残りの領域を結合する転写後プロセス。
*2 RANKL
骨細胞や骨芽細胞の表面に発現している膜貫通タンパク質の1種。破骨細胞の前駆細胞は、その表面に膜貫通タンパク質「RANK」を発現しており、RANKLが結合することで活性化され、破骨細胞に分化する。
*3 ポリアクリルアミド電気泳動(SDS-PAGE)
分子量の差を利用してタンパク質を分離する手法。
*4 トランスフェクション
ウイルスを用いない方法で細胞にDNAまたはRNAを導入する手法。
*5 液—液相分離
濃度の異なる2種類の液体が水と油のように分離する現象。物理化学分野では古くから知られている現象だが、近年、細胞内でも一般的に生じている現象であることがわかりつつある。
*6 細胞質液滴
液—液相分離によって細胞質内に形成される液滴。細胞質液滴の内部には特定の分子が凝集し、細胞機能の制御に関わるはたらきを担う。
【論文情報】
雑誌名:Journal of Cellular Physiology
論文タイトル:The RNA-binding protein Cpeb4 regulates splicing of the Id2 gene in osteoclast differentiation
著者:Yasuhiro Arasaki and Tadayoshi Hayata
DOI:10.1002/jcp.31197
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
