認知機能亢進作用に対する内因性オキシトシンの影響を神経回路レベルで解明
~認知症治療の新たな道を切り拓く~
【研究の要旨とポイント】
本研究グループは、愛情ホルモンとして知られるオキシトシンが、アルツハイマー型認知症の治療薬候補として有望であることを2020年に世界で初めて報告し、臨床応用を目指して研究を進めています。
しかし、内因性オキシトシンが認知機能に与える生理的影響についてはまだよくわかっていません。
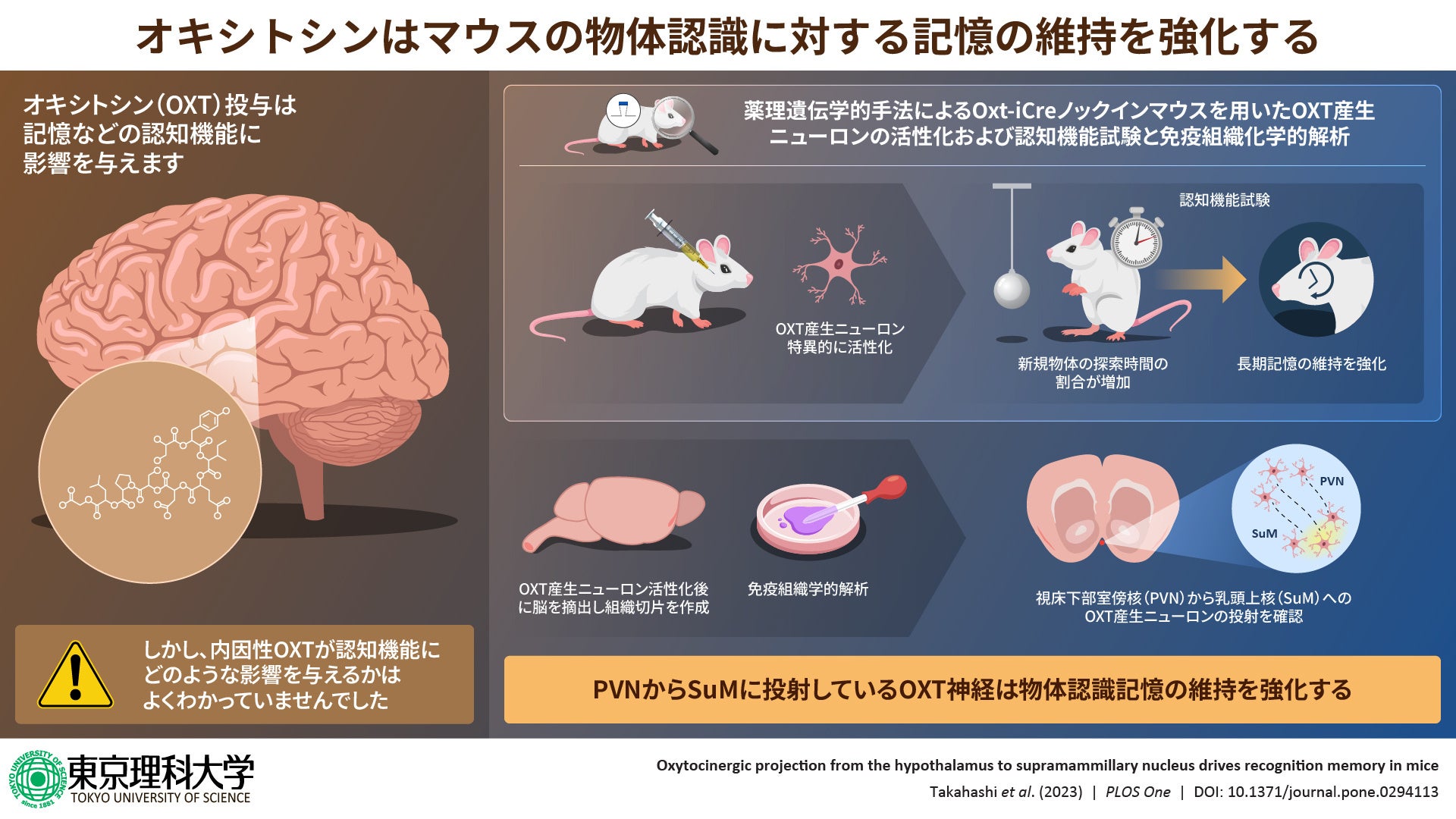
本研究では、視床下部室傍核から乳頭上核に投射しているオキシトシン産生ニューロンが認知機能亢進作用に関与していることを明らかにしました。
本研究成果は認知症治療の新たな指針となり、将来的には治療法や薬剤の開発につながることが期待されます。
【研究の概要】
東京理科大学 薬学部薬学科の斎藤 顕宜教授、同大学大学院 薬学研究科薬科学専攻の高橋 純平氏(2023年度 博士課程3年)らの研究グループは、薬理遺伝学的手法を用いて認知機能における内因性オキシトシンの役割を調べ、視床下部室傍核(PVN)から乳頭上核(SuM)に投射しているオキシトシン産生ニューロンがオキシトシンの認知機能亢進作用に深く関与していることを発見しました。
オキシトシン産生ニューロンは脳内のさまざまな領域に投射し、神経回路を形成しています。これまで外因性オキシトシンが認知機能に及ぼす影響については数多く報告されていますが、内因性オキシトシンの具体的な役割については明らかにされていませんでした。そこで本研究では、マウス実験により内因性オキシトシンの認知機能における役割の解明に取り組みました。
マウスにクロザピン-N-オキシド(CNO, *1)を投与してオキシトシン産生ニューロンを活性化し、新規物体認識試験(*2)による物体認識記憶の変化と、免疫組織化学染色によるc-Fos(*3)の発現を評価し、神経活動の詳細な観察を行いました。その結果、CNO投与を受けたマウスでは、新規物体の探索時間の割合が増加し、SuM内のc-Fos陽性細胞数も有意に増加することがわかりました。また、PVNからSuMに伸びるオキシトシン陽性線維が確認され、SuMにCNOを局所的に投与することで、新規物体の探索時間が大幅に増加することも判明しました。以上の結果から、PVNのオキシトシン産生ニューロンがSuMに投射することで、マウスの物体認識記憶が調節される可能性が示唆されました。本研究成果をさらに発展させることにより、認知症の進行を防ぐ治療薬への応用が期待されます。
本研究成果は、2023年11月16日に国際学術誌「PLOS One」にオンライン掲載されました。
【研究の背景】
オキシトシンは愛情ホルモン、幸せホルモンとも呼ばれ、他者との交流によって活性化されることが知られています。最近の研究から、オキシトシンが認知機能低下の改善に有効であることもわかってきています。一般的に、孤独や社会的な孤立状態が認知症の進行に負の影響を与える可能性が指摘されていますが、オキシトシンの影響を含めた生理学的なメカニズムについては、ほとんど明らかにされていませんでした。
近年、本研究グループは、アミロイドβ(Aβ, *4)を脳室内に投与することによってアルツハイマー型認知症モデルマウスの空間記憶障害がオキシトシンにより回復したことを報告し、オキシトシンが認知症に対する新たな治療薬の候補として有望であることを示しました(※1, 2)。これらの研究成果では、オキシトシン産生ニューロンの神経活動が認知症の病理学的進行の各プロセスに関与している可能性が示唆されましたが、内因性オキシトシンが認知機能に与える影響はまだ十分に研究されておらず、オキシトシン産生ニューロンが認知機能に与える直接的な影響についてはまだ解明されていません。
そこで本研究グループは、薬理遺伝学的手法を用い、PVNでオキシトシン産生ニューロンを特異的に活性化させることで、オキシトシンの認知機能亢進作用について、神経回路レベルで明らかにしようと試みました。
*1: 東京理科大学プレスリリース
『オキシトシン経鼻投与でアルツハイマー型認知症に関連する認知行動障害を改善 ~アルツハイマー型認知症の新たな治療薬開発へ一歩前進~』
URL: https://www.tus.ac.jp/today/archive/20221024_5682.html
*2: 東京理科大学プレスリリース
『オキシトシンがアルツハイマー型認知症に関連する神経活性の障害を改善 ~新たな作用機序を有するアルツハイマー型認知症の治療薬開発に期待~』
URL: https://www.tus.ac.jp/today/archive/20200710_2987.html
【研究結果の詳細】
はじめに、PVN内のオキシトシン産生ニューロンの投射を受け取る脳領域を調査しました。PVNにウイルス(AAV8-hSyn-DIO-hM3Dq-mCherry)を投与したマウスを用いて、蛍光タンパク質であるmCherryの発現を分析しました。結果として、PVNでmCherry陽性細胞、SuMでmCherry陽性線維が確認され、PVNのオキシトシンニューロンがSuMに投射していることが示唆されました。一方で、学習や記憶と深く関係する海馬ではmCherry陽性線維は確認されませんでした。
次に、アデノ随伴ウィルス(AAV)ベクターを用いて、興奮性DREADD(hM3Dq)をオキシトシン-iCreノックインマウス(オキシトシン特異的にCreリコンビナーゼ(*5)を発現するマウス)に発現させ、CNOの投与によりオキシトシン産生ニューロンが活性化されるかどうかを調べました。その結果、CNOの投与により、PVN内のc-Fos陽性細胞数が有意に増加していることがわかりました。また、免疫蛍光染色によってc-Fos陽性ニューロンがオキシトシン産生ニューロンであることが確認されました。
その後、PVN内の活性化したオキシトシン産生ニューロンが学習と記憶に与える影響をY字迷路試験と新規物体探索試験で評価しました。これらの試験の結果、内因性オキシトシンは短期的な空間記憶にはほとんど影響しないことが示唆されました。一方、新規物体認識試験においてはCNOを投与したマウスが新規物体の探索時間を増加させたことから、内因性オキシトシンが長期の物体認識記憶を強化する可能性が示唆されました。
最後に、新規物体認識試験後のc-Fos染色を確認し、物体認識記憶の強化に関与する脳領域を調査しました。その結果、CNOを投与したマウスでは海馬歯状回とSuMのc-Fos陽性細胞の数が有意に増加していることを見出しました。これは、オキシトシン産生ニューロンの活性化が、海馬歯状回やSuMのニューロンを介してマウスの長期記憶の維持を強化する可能性を示唆しています。海馬歯状回ニューロンやSuMニューロンを活性化することで、オキシトシン産生ニューロンが活性化され、物体認識記憶が強化されると考えられます。
本研究を主導した斎藤教授は「私たちの研究グループは世界で初めて、オキシトシンが認知機能を亢進させることを明らかにしました。家族との交流が少なくなった環境で認知症が急速に進行することは経験的によく知られていることですが、その背景にオキシトシンが関係しているのではないかと考えたのが本研究をはじめたきっかけです。今回、内因性オキシトシンの認知症亢進について、神経回路レベルでのメカニズムを見出すことができました。この研究を発展させることで、認知症の進行を防ぐ新しい治療法・治療薬の開発につながることが期待されます」と、研究成果についてコメントしています。
※本研究は、日本学術振興会(JSPS)の特別研究員奨励費(JP21J20036)の助成を受けて実施したものです。
【用語】
*1 クロザピン-N-オキシド(CNO)
DREADD(Designer Receptors Exclusively Activated by Designer Drugs, デザイナードラッグによってのみ活性化されるデザイナー受容体)などの遺伝子改変されたGタンパク質共役型受容体を活性化する。
*2 新規物体認識試験
認知機能の評価手法の一つ。マウスに2つの物体を提示して探索させた後、片方を新しい物体に置き換える試験で、認知機能が正常に機能している場合、新しい物体を探索する時間が相対的に長くなる。新しい物体を認識し、記憶する能力を評価するのに利用される。
*3 c-Fos
細胞内の転写因子としての機能を有するタンパク質。神経活動とも深く関連しており、c-Fosの発現を調べることで、特定の刺激や反応が及ぼす影響を知ることができる。
*4 アミロイドβ(Aβ)
脳内に蓄積することでアルツハイマー型認知症の原因となるタンパク質。
*5 Creリコンビナーゼ
DNA組換え反応を触媒する酵素の1つで、34塩基から成るDNA配列(loxP)に結合し、部位特異的に組換えを起こす。
【論文情報】
雑誌名:PLOS One
論文タイトル:Oxytocinergic projection from the hypothalamus to supramammillary nucleus drives recognition memory in mice
著者:Junpei Takahashi, Daisuke Yamada, Wakana Nagano, Yoshitake Sano, Teiichi Furuichi, Akiyoshi Saitoh
DOI:10.1371/journal.pone.0294113
このプレスリリースには、メディア関係者向けの情報があります
メディアユーザー登録を行うと、企業担当者の連絡先や、イベント・記者会見の情報など様々な特記情報を閲覧できます。※内容はプレスリリースにより異なります。
すべての画像
